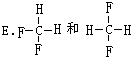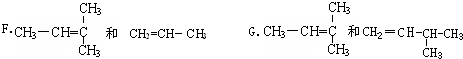题目内容
(1)新制备的氯水显 色,说明氯水中有 (填分子式)分子存在.
(2)向氯水中滴加几滴AgNO3溶液,立即有 生成,说明氯水中有 (填离子符号)存在,反应的化学方程式为 .
(3)氯水光照后颜色变浅,并放出 气体.
(4)相同物质的量 的SO2气体和SO3气体,其分子数之比为 ,相同质量的SO2气体和SO3气体,其分子数之比为 .
(2)向氯水中滴加几滴AgNO3溶液,立即有
(3)氯水光照后颜色变浅,并放出
(4)相同物质的量 的SO2气体和SO3气体,其分子数之比为
考点:氯气的化学性质
专题:卤族元素
分析:(1)新制备的氯水中氯气和水反应生成盐酸和次氯酸,反应是化学平衡;
(2)向氯水中滴加几滴AgNO3溶液生成白色沉淀氯化银,说明氯水中含有氯离子;
(3)氯水中次氯酸见光分解生成氧气和盐酸;
(4)依据气体一定条件下等物质的量的气体物质的量相同,分子数相同;相同质量的气体依据n=
计算物质的量得到分子数.
(2)向氯水中滴加几滴AgNO3溶液生成白色沉淀氯化银,说明氯水中含有氯离子;
(3)氯水中次氯酸见光分解生成氧气和盐酸;
(4)依据气体一定条件下等物质的量的气体物质的量相同,分子数相同;相同质量的气体依据n=
| m |
| M |
解答:
解:(1)新制备的氯水中氯气和水反应生成盐酸和次氯酸,反应是化学平衡,Cl2+H2O?HCl+HClO,氯水中含有氯气分子,溶液呈浅黄绿色;
故答案为:浅黄绿色;Cl2;
(2)向氯水中滴加几滴AgNO3溶液生成白色沉淀氯化银,说明氯水中含有氯离子,反应的离子方程式为:Ag++Cl-=AgCl↓;
故答案为:白色沉淀;Cl-;Ag++Cl-=AgCl↓;
(3)氯水光照后颜色变浅,氯水中次氯酸见光分解生成氧气和盐酸2HClO
2HCl+O2,故答案为:O2;
(4)依据气体一定条件下等物质的量的气体物质的量相同,分子数相同,相同物质的量 的SO2气体和SO3气体,其分子数之比为1:1;相同质量的气体依据n=
计算物质的量得到分子数=
:
=5:4;
故答案为:1:1;5:4.
故答案为:浅黄绿色;Cl2;
(2)向氯水中滴加几滴AgNO3溶液生成白色沉淀氯化银,说明氯水中含有氯离子,反应的离子方程式为:Ag++Cl-=AgCl↓;
故答案为:白色沉淀;Cl-;Ag++Cl-=AgCl↓;
(3)氯水光照后颜色变浅,氯水中次氯酸见光分解生成氧气和盐酸2HClO
| ||
(4)依据气体一定条件下等物质的量的气体物质的量相同,分子数相同,相同物质的量 的SO2气体和SO3气体,其分子数之比为1:1;相同质量的气体依据n=
| m |
| M |
| 1 |
| 64 |
| 1 |
| 80 |
故答案为:1:1;5:4.
点评:本题考查了氯气性质的分析判断,掌握氯气及其化合物性质是解题关键,题目较简单.

练习册系列答案
相关题目
铝-空气电池具有体积小、能量大,污染少等优点,是电动自行车和电动汽车比较理想的电源.电池以食盐水为电解液,总反应为:4Al+3O2+6H2O=4Al(OH)3↓下列说法中正确的是( )
| A、电池工作时,铝做正极 |
| B、电池负极的电极反应式为:3O2+6H2O+12e-=12OH- |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、外电路中每通过1mole-,铝的质量理论上减小9g |
下列褪色过程不是因为氧化还原反应而褪色的是( )
| A、SO2气体通入溴水使溴水褪色 |
| B、氯水使滴有酚酞的NaOH溶液褪色,加入NaOH后不变红 |
| C、将苯滴入溴水中振荡,溴水层褪色 |
| D、将含有碘单质的淀粉溶液,加入NaOH溶液后蓝色褪去 |
下列有关说法不正确的是( )
| A、服用铬含量超标的药用胶囊会对人对健康造成危害 |
| B、食用一定量的油脂能促进人体对某些维生素的吸收 |
| C、明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| D、镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
下列叙述正确的是( )
| A、结合质子(H+)能力:OH->CH3COO->Cl- |
| B、除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| C、F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
| D、X、Y均为短周期元素,其简单离子mXa+与nYb-的电子层结构相同,则m+a=n-b |
 (1)T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),平衡时c(CH4)=0.5mol?L-1.该温度下反应CH4(g)+H2O(g)?CO(g)+3H2(g)的平衡常数K=
(1)T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),平衡时c(CH4)=0.5mol?L-1.该温度下反应CH4(g)+H2O(g)?CO(g)+3H2(g)的平衡常数K=