题目内容
11.在0.1mol/L NH4NO3溶液中,离子浓度最大的是( )| A. | NO3- | B. | NH4+ | C. | H+ | D. | OH- |
分析 在0.1mol/L NH4NO3溶液中,铵根离子水解,溶液显酸性.
解答 解:在0.1mol/L NH4NO3溶液中,铵根离子水解,NH4++H2O?NH3•H2O+H+,铵根离子浓度小于0.1mol/L,硝酸根离子浓度等于0.1mol/L,离子浓度最大的是硝酸根离子,故选A.
点评 本题考查了盐类水解的分析,主要是离子浓度大小比较,题目难度不大.

练习册系列答案
相关题目
19.下列变化属于物理变化的是( )
| A. | 铁粉燃烧 | B. | 铁钉生锈 | C. | 石碱风化 | D. | 碘的萃取 |
6. 实验室制取氢气所用粗锌中多含有杂质铜,某小组同学利用如图装置测定粗锌中锌的质量分数,每隔相同时间读得电子天平的数据如表:(已知粗锌质量为1.950g、锥形瓶和稀盐酸的质量为190.720g)
实验室制取氢气所用粗锌中多含有杂质铜,某小组同学利用如图装置测定粗锌中锌的质量分数,每隔相同时间读得电子天平的数据如表:(已知粗锌质量为1.950g、锥形瓶和稀盐酸的质量为190.720g)
(1)写出锌和盐酸反应的化学方程式Zn+2HCl→ZnCl2+H2↑.
(2)不必作第6次读数的原因是第五次数据已达恒重,说明反应完全了.计算粗锌的质量分数时,需用到的数据有试样质量(或1.950 g)、锥形瓶加盐酸的质量(或190.720 g)、第4(或5)次读数(或192.610 g).
(3)数据处理结束后,同学们发现他们的测定结果明显偏大(填偏大、偏小或不变).他们在锥形瓶上增加一个装有碱石灰的干燥管后,再次实验,得到了较正确的结果.干燥管的作用有吸收水蒸气、吸收氯化氢气体.
 实验室制取氢气所用粗锌中多含有杂质铜,某小组同学利用如图装置测定粗锌中锌的质量分数,每隔相同时间读得电子天平的数据如表:(已知粗锌质量为1.950g、锥形瓶和稀盐酸的质量为190.720g)
实验室制取氢气所用粗锌中多含有杂质铜,某小组同学利用如图装置测定粗锌中锌的质量分数,每隔相同时间读得电子天平的数据如表:(已知粗锌质量为1.950g、锥形瓶和稀盐酸的质量为190.720g)| 读数次数 | 质量(g) | |
| 锥形瓶 + 稀盐酸 + 粗锌 | 第1次 | 192.655 |
| 第2次 | 192.636 | |
| 第3次 | 192.620 | |
| 第4次 | 192.610 | |
| 第5次 | 192.610 |
(2)不必作第6次读数的原因是第五次数据已达恒重,说明反应完全了.计算粗锌的质量分数时,需用到的数据有试样质量(或1.950 g)、锥形瓶加盐酸的质量(或190.720 g)、第4(或5)次读数(或192.610 g).
(3)数据处理结束后,同学们发现他们的测定结果明显偏大(填偏大、偏小或不变).他们在锥形瓶上增加一个装有碱石灰的干燥管后,再次实验,得到了较正确的结果.干燥管的作用有吸收水蒸气、吸收氯化氢气体.
3.下列离子在溶液中能大量共存的一组是( )
| A. | Na+、Al3+、Cl-、OH- | B. | Na+、H+、OH-、Cl- | ||
| C. | NH4+、Mg2+、SO42-、Cl- | D. | Na+、Cl-、AlO2-、H+ |
1.物质的量浓度相同的下列物质的水溶液,pH最小的是( )
| A. | Na2CO3 | B. | NH4Cl | C. | H2SO4 | D. | CH3COOH |
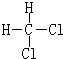 或
或 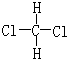
 .氟元素最低负化合价为-1 价.
.氟元素最低负化合价为-1 价. .
.