题目内容
16.小明在实验室电解水,如果电解产生了标准状况下44.8L的氧气,则:①电解水的质量是多少?
②电解产生另外一种气体的物质的量?
分析 n(O2)=$\frac{44.8L}{22.4L/mol}$=2mol,结合2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑计算.
解答 解:电解水生成标准状况下44.8L的氧气,n(O2)=$\frac{44.8L}{22.4L/mol}$=2mol,
①由2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑可知,需要4molH2O反应,则电解水的质量是4mol×18g/mol=72g,
答:电解水的质量是72g;
②由2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑可知,电解产生另外一种气体的物质的量为2mol×2=4mol,
答:电解产生另外一种气体的物质的量为4mol.
点评 本题考查电解反应的计算,为高频考点,把握发生电解反应、物质的量关系为解答的关键,侧重分析与计算能力的考查,注意物质的量的相关计算,题目难度不大.

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
5.元素周期律和元素周期表是学习化学的重要工具,下列说法正确的是( )
| A. | 第IA族元素的金属性一定比第ⅡA族元素的金属性强 | |
| B. | 第VIIA族元素从上到下,其氢化物的还原性依次减弱 | |
| C. | 第三周期从左到右,非金属元素最高价氧化物对应的水化物的酸性依次增强 | |
| D. | 第三周期元素的离子半径从左到右逐渐减小 |
6.Mg(OH)2可用作塑料的阻燃剂.现以某矿石(主要成分为3MgO•2SiO2•2H2O,还有少量Fe2O3、FeO、CaO和Al2O3)为原料生产,其工艺流程如下:
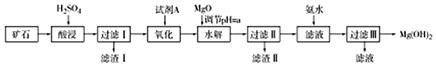
已知:
表1生成氢氧化物沉淀的pH
表2原料价格表
回答下列问题:
(1)酸浸时,为提高矿石的浸出率可采取的措施为将矿石粉碎(任写一条).该过程H2SO4适当过量的目的是使固体充分溶解、使Ca2+以CaSO4沉淀形式除去.
(2)工业生产要求生产成本较低,产品尽量不含杂质.试剂A的最佳选择是漂液(或NaClO),写出其发生反应的离子方程式2Fe2++ClO-+2H+=2Fe3++Cl-+H2O.
(3)水解过程需调节溶液pH,a的取值范围为4.7≤a<9.1,滤渣II的成分是Fe(OH)3、Al(OH)3(填化学式).
(4)向过滤II所得滤液中加入一定量氨水,写出镁离子沉淀的离子方程式Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+,该过程温度不宜过高的原因是氨水受热分解.
(5)实际生产中,可由Mg(OH)2为原料制备单质镁,简述制备方法Mg(OH)2与盐酸反应生产MgCl2,蒸发浓缩冷却结晶得到MgCl2•6H2O晶体,在HCl气流中加热失水得到无水MgCl2,电解熔融的MgCl2制取金属Mg.

已知:
表1生成氢氧化物沉淀的pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 7.6 | 1.9 | 3.4 | 9.1 |
| 完全沉淀的pH | 9.6 | 3.2 | 4.7 | 11.1 |
| 物质 | 价格(元•吨-1) |
| 漂液(含25.2% NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
(1)酸浸时,为提高矿石的浸出率可采取的措施为将矿石粉碎(任写一条).该过程H2SO4适当过量的目的是使固体充分溶解、使Ca2+以CaSO4沉淀形式除去.
(2)工业生产要求生产成本较低,产品尽量不含杂质.试剂A的最佳选择是漂液(或NaClO),写出其发生反应的离子方程式2Fe2++ClO-+2H+=2Fe3++Cl-+H2O.
(3)水解过程需调节溶液pH,a的取值范围为4.7≤a<9.1,滤渣II的成分是Fe(OH)3、Al(OH)3(填化学式).
(4)向过滤II所得滤液中加入一定量氨水,写出镁离子沉淀的离子方程式Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+,该过程温度不宜过高的原因是氨水受热分解.
(5)实际生产中,可由Mg(OH)2为原料制备单质镁,简述制备方法Mg(OH)2与盐酸反应生产MgCl2,蒸发浓缩冷却结晶得到MgCl2•6H2O晶体,在HCl气流中加热失水得到无水MgCl2,电解熔融的MgCl2制取金属Mg.
4.n克的H2SO4所含氧原子的物质的量是( )
| A. | $\frac{n}{98}$moL | B. | $\frac{7n}{98}$moL | C. | $\frac{4n}{98}$moL | D. | $\frac{4n}{32}$moL |
11.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下,1 L 0.1 mol/L的NH4NO3溶液中氢原子总数为0.4NA | |
| B. | 0.5 mol 甲基中电子数为5NA | |
| C. | 在反应3Br2+3CO32-=5Br-+BrO3-+3CO2↑中,每生成3 mol CO2转移的电子数为5NA | |
| D. | 常温常压下,22.4 L N2H4中N-H键数为4NA |
1.多原子分子氰[(CN)2]、硫氰[(SCN)2]和(OCN)2的性质与卤素单质相似,故称它们为类卤素,它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I).
(1)在表中①、②、③的空格处应填写的名称或化学式分别是氧氰、HSCN、KOCN.
(2)完成下列反应的化学方程式或离子方程式.
①(CN)2和KOH溶液反应的化学方程式为(CN)2+2KOH═KCN+KCNO+H2O.
②已知阴离子的还原性:Cl-<Br-<CN-<SCN-<I-.试写出在NaBr和KSCN的混合溶液中加入(CN)2时发生反应的离子方程式:(CN)2+2SCN-═2CN-+(SCN)2.
| 卤素 | 氰 | 硫氰 | ① | |
| “单质” | X2 | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 盐 | KX | KCN | KSCN | ③ |
(2)完成下列反应的化学方程式或离子方程式.
①(CN)2和KOH溶液反应的化学方程式为(CN)2+2KOH═KCN+KCNO+H2O.
②已知阴离子的还原性:Cl-<Br-<CN-<SCN-<I-.试写出在NaBr和KSCN的混合溶液中加入(CN)2时发生反应的离子方程式:(CN)2+2SCN-═2CN-+(SCN)2.
6.下列实验操作或对实验相关的描述,正确的是( )
| A. | 皮肤上不慎沾到少量浓硫酸,应先用干抹布擦拭、再用大量水冲洗 | |
| B. | 检验HCl气体中是否混有Cl2,可将气体通入硝酸银溶液 | |
| C. | 验证某气体中含CO2、SO2,可依次通入品红溶液、饱和NaHCO3溶液、澄清石灰水 | |
| D. | 检验Fe2(SO4)3溶液中是否含有Fe2+,可用KMnO4酸性溶液 |
 ;化合物BA4的电子式为
;化合物BA4的电子式为 .
.