题目内容
用下列各组仪器或装置,不能达到实验目的是( )


| A、a组:制备少量乙酸乙酯 |
| B、b组:除去粗盐水中的泥沙 |
| C、c组:用CCl4提取碘水中的碘 |
| D、d组:配制100 mL 1.00 mol/L NaCl溶液 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.加热试管中为乙酸、乙醇、浓硫酸,右侧试管中盛放碳酸钠溶液;
B.泥沙不溶于水,可过滤分离;
C.碘不易溶于水,易溶于四氯化碳,混合后分层;
D.配制100 mL 1.00 mol/L NaCl溶液.一定需要100mL容量瓶.
B.泥沙不溶于水,可过滤分离;
C.碘不易溶于水,易溶于四氯化碳,混合后分层;
D.配制100 mL 1.00 mol/L NaCl溶液.一定需要100mL容量瓶.
解答:
解:A.加热试管中为乙酸、乙醇、浓硫酸,右侧试管中盛放碳酸钠溶液,图中装置可制备少量乙酸乙酯,故A正确;
B.泥沙不溶于水,可过滤分离,图中过滤装置可除去粗盐水中的泥沙,故B正确;
C.碘不易溶于水,易溶于四氯化碳,混合后分层,图中分液装置可用CCl4提取碘水中的碘,故C正确;
D.配制100 mL 1.00 mol/L NaCl溶液.一定需要100mL容量瓶,图中缺少容量瓶,不能完成实验,故D错误;
故选D.
B.泥沙不溶于水,可过滤分离,图中过滤装置可除去粗盐水中的泥沙,故B正确;
C.碘不易溶于水,易溶于四氯化碳,混合后分层,图中分液装置可用CCl4提取碘水中的碘,故C正确;
D.配制100 mL 1.00 mol/L NaCl溶液.一定需要100mL容量瓶,图中缺少容量瓶,不能完成实验,故D错误;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质的制备、混合物分离提纯及溶液的配制等,注重实验装置图作用及物质性质的考查,注意实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
化学与人类生产、生活、社会可持续发展密切相关.下列说法正确的是( )
| A、减少CO2的排放,可以减少酸雨的产生 |
| B、减少SO2的排放,可以从根本上消除雾霾 |
| C、“天宫一号”使用的碳纤维,是一种新型有机高分子材料 |
| D、用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 |
如图实验操作正确的是( )
A、 称量氢氧化钠固体 |
B、 配制150mL 0.10mol/L盐酸 |
C、 检验铁粉与水蒸气反应产生的氢气 |
D、 分离两种互溶但沸点相差较大的液体混合物 |
下列有关环境方面的说法不正确的是( )
| A、采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 |
| B、采用天然石材装修家居,可减轻室内甲醛污染但会导致一定量的放射性物质的污染 |
| C、汽油中添加含铅化合物Pb(C2H5)4,可提高汽油的抗爆震性能,有利于改善大气环境 |
| D、PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重 |
对反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,下列判断不正确的是( )
| A、该反应的还原剂是Cu2S |
| B、当1mol O2发生反应时,还原剂所失去电子的物质的量为4mol |
| C、O2发生了氧化反应 |
| D、CuSO4即是氧化产物,又是还原产物 |

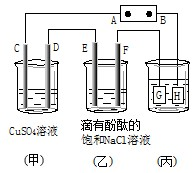 如图装置所示,C、D、E、F都是惰性电极,
如图装置所示,C、D、E、F都是惰性电极,