题目内容
下列叙述正确的是( )
| A、mol是物质的质量的单位 |
| B、mol是物质的量的单位 |
| C、阿伏加德罗常数没有单位 |
| D、摩尔质量的不是物理量,所以没有单位 |
考点:物质的量的单位--摩尔,摩尔质量,阿伏加德罗常数
专题:
分析:物质的量是国际单位制中的七个基本物理量之一,其单位为mol,阿伏伽德罗常数的单位为mol-1,摩尔质量不是基本物理量,但摩尔质量是物理量,其单位为g/mol,据此进行解答.
解答:
解:A.物质质量的单位为g,mol是物质的量的单位的符号,故A错误;
B.物质的量是国际单位制中的七个基本物理量之一,且单位为摩尔,符号为mol,故B正确;
C.阿伏伽德罗常数有单位,单位为mol-1,故C错误;
D.摩尔质量是物理量,其单位为g/mol,故D错误;
故选B.
B.物质的量是国际单位制中的七个基本物理量之一,且单位为摩尔,符号为mol,故B正确;
C.阿伏伽德罗常数有单位,单位为mol-1,故C错误;
D.摩尔质量是物理量,其单位为g/mol,故D错误;
故选B.
点评:本题考查了物质的量与摩尔的关系、摩尔质量与质量、阿伏伽德罗常数的判断,题目难度不大,试题侧重基础知识的考查,注意明确物质的、摩尔质量、阿伏伽德罗常数的概念,明确物质的量与摩尔的关系及摩尔质量与质量的区别.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列溶液中Cl-的物质的量浓度与100ml 1mol?L-1AlCl3溶液中Cl-相等的是( )
| A、150ml 1 mol?L-1氯化钠溶液 |
| B、75ml 2 mol?L-1氯化镁溶液 |
| C、50ml 3mol?L-1氯化钾溶液 |
| D、200ml 1.5 mol?L-1氯化铁溶液 |
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的碳原子数目之比为1:1.
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的碳原子数目之比为1:1.
| A、①和④ | B、②和③ |
| C、③和④ | D、①②③④ |
设NA为阿伏伽德罗常数的数值,则下列说法中正确的是( )
①2.24L氨气含有NA个电子,
②1.4g乙烯与丙烯的混合气体含有NA个碳原子,
③精炼铜,若阳极失去2NA个电子,则阴极增重64g,
④标准状况下,22.4L空气含有NA个分子,
⑤过氧化钠与水反应,若电子转移4NA,则产生的氧气为64g,
⑥将1L 2mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA,
⑦在12g石墨晶体中,含有非极性键的数目为1.5NA.
①2.24L氨气含有NA个电子,
②1.4g乙烯与丙烯的混合气体含有NA个碳原子,
③精炼铜,若阳极失去2NA个电子,则阴极增重64g,
④标准状况下,22.4L空气含有NA个分子,
⑤过氧化钠与水反应,若电子转移4NA,则产生的氧气为64g,
⑥将1L 2mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA,
⑦在12g石墨晶体中,含有非极性键的数目为1.5NA.
| A、③⑤④⑦ | B、①③④⑦ |
| C、②③④⑤⑦ | D、②④⑤⑦ |
下列说法中不正确的是( )
| A、σ键比π键的电子云重叠程度大,形成的共价键强 |
| B、C=C双键的键能是C-C单键键能的2倍 |
| C、s-s σ键与s-p σ键的电子云形状对称性相同 |
| D、N2分子中有一个σ键,2个π键 |
下列关于分散系的说法,正确的是( )
| A、稀硫酸是分散系 |
| B、分散质一定是固体 |
| C、分散剂一定是液态 |
| D、分散系一定是液态 |
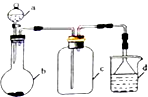 根据如图装置和表中提供的物质完成实验室制取、收集表中气体并进行尾气处理 (省略夹持、加热及净化装置),最合理的选项是( )
根据如图装置和表中提供的物质完成实验室制取、收集表中气体并进行尾气处理 (省略夹持、加热及净化装置),最合理的选项是( )