题目内容
下列说法正确的是:
A、过量的铁在氯气中燃烧可生成氯化亚铁
B、向Fe(NO3)2溶液加入盐酸,由于酸性增强抑制Fe2+的水解,使c(Fe2+)增大
C、Fe和Fe2O3的混合物溶于盐酸中,再加入KSCN溶液,溶液一定变为血红色
D、把一定量的铁和铜的混和粉未投入到FeCl3溶液中,不可能出现只有铁剩余没有铜剩余的情况
D
【解析】
试题分析:由于Cl2强氧化性,与铁反应不论过量与否均生成氯化铁,故A错误;向Fe(NO3)2溶液加入盐酸,酸性条件下的硝酸根具有强氧化性,会氧化Fe2+为Fe3+,溶液中C(Fe2+)减小,故B项错误;Fe和Fe2O3的混合物溶于盐酸中,Fe和Fe3+会发生氧化还原反应Fe+ 2Fe3+==3 Fe2+,若溶液中恰好为Fe2+,加入KSCN溶液,溶液不变为血红色,故C项错误;把一定量的铁和铜的混和粉未投入到FeCl3溶液中,铁的还原性强于铜,所以若有铁剩余,则铜一定未参与反应,必然会剩余,所以不可能出现只有铁剩余没有铜剩余的情况,故D项正确。
考点:铁及其化合物知识

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
下列说法正确的是
| A.摩尔是七个基本物理量之一 |
| B.阿伏伽德罗常数是没有单位的 |
| C.氮气的摩尔质量是28g |
| D.1molH2O约含有6.02×1023个水分子 |





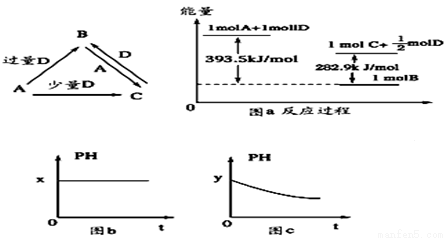
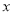 ________7(填“﹥”“﹤”“=”)。若图c符合事实,则其pH变化的原因是_____________(用离子方程式表示)。
________7(填“﹥”“﹤”“=”)。若图c符合事实,则其pH变化的原因是_____________(用离子方程式表示)。