题目内容
6.下列实验操作正确的是( )| A. |  称NaOH固体的质量 | B. | 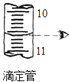 读数为10.60 | ||
| C. | 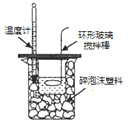 反应热的测定 | D. | 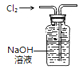 收集氯气 |
分析 A.称量NaOH固体时应该遵循“左物右砝”原则,且氢氧化钠应该盛放在烧杯中;
B.滴定管的感量是0.01mL;
C.反应热的测定中温度计应该测定混合溶液温度;
D.氯气能和NaOH反应,所以不能用排NaOH溶液方法收集氯气.
解答 解:A.称量NaOH固体时应该遵循“左物右砝”原则,氢氧化钠具有强腐蚀性且易潮解,所以氢氧化钠应该盛放在烧杯中,故A错误;
B.滴定管的感量是0.01mL,所以读数为10.60,故B正确;
C.反应热的测定中温度计应该测定混合溶液温度,故C错误;
D.氯气能和NaOH反应,所以不能用排NaOH溶液方法收集氯气,可以采用向上排空气法收集氯气,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及气体收集、仪器使用、实验基本操作等知识点,明确实验基本操作方法、气体收集方法是解本题关键,注意滴定管感量,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得下列说法正确的是( )


| A. | 可用FeCl3溶液检验C中是否含有B | |
| B. | 1molC分子最多可与4molH2发生加成反应 | |
| C. | 可以用酸性KMnO4溶液检验B中是否含有-CHO | |
| D. | 1molC与NaOH溶液反应时最多消耗1molNaOH |
15.向密度为d g•cm-3的盐酸中逐滴加入硝酸银溶液到过量,生成沉淀的质量与原盐酸的质量相等,原盐酸的物质的量浓度为( )
| A. | 25.4d mol•L-1 | B. | 12.7d mol•L-1 | C. | 6.97d mol•L-1 | D. | 6.35d mol•L-1 |
16.下列物质中,发生消去反应生成的烯烃只有一种的是( )
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |

 ,它们的单质都必须采用电解法制备,但都无需密封保存,
,它们的单质都必须采用电解法制备,但都无需密封保存, .(2)Y元素在周期表中位置第三周期ⅢA族.
.(2)Y元素在周期表中位置第三周期ⅢA族. ,X、Y的最高价含氧酸的浓溶液都有强氧化性.
,X、Y的最高价含氧酸的浓溶液都有强氧化性.