题目内容
7.标准状况下,8.8gCO2所占体积约为( )| A. | 5.6L | B. | 22.4L | C. | 11.2L | D. | 4.48L |
分析 标准状况下,Vm=22.4 L/mol,根据n=$\frac{m}{M}$计算出8.8gCO2的物质的量,然后带入V=n•Vm计算体积.
解答 解:8.8gCO2的物质的量n=$\frac{8.8g}{44g/mol}$=0.2mol,标准状况下,Vm=22.4 L/mol,V=n•Vm=0.2mol×22.4 L/mol=4.48L,
故选:D.
点评 本题考查了物质的量的相关计算,难度不大,熟练应用n=$\frac{m}{M}$和V=n•Vm即可解答,侧重考查学生对基础知识掌握熟练程度.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列反应中,属于取代反应的是( )
| A. | 苯在溴化铁存在时与溴反应 | B. | 苯在空气中燃烧 | ||
| C. | 苯在镍做催化剂时与氢气反应 | D. | 苯与溴水混合后分层 |
18.下列表示物质的图或式正确的是( )
| A. | 氮气的电子式 | B. | Mg2+的结构示意图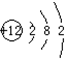 | ||
| C. | NH3的结构式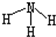 | D. | 二氧化碳的电子式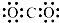 |
15.根据下列微粒的最外层电子排布,能确定该元素在元素周期表中位置的是( )
| A. | 1s2 | B. | 3s23p1 | C. | 2s22p6 | D. | ns2np3 |
2.下列物质中羟基氢原子的活动性由强到弱的顺序正确的是( )
①水 ②乙醇 ③苯酚 ④碳酸.
①水 ②乙醇 ③苯酚 ④碳酸.
| A. | ①②③④ | B. | ①③②④ | C. | ④③②① | D. | ④③①② |
12.下列有关实验操作、现象和解释或结论都正确的是( )
| 实验操作 | 现象 | 解释或结论 | |
| A | 将等体积的CH4和Cl2装入硬质大试管混合后,再将试管倒置于饱和食盐水中,在漫射光的照射下充分反应 | 试管内气体颜色逐渐变浅,试管内壁出现油状液滴 | 甲烷与氯气在光照条件下发生了取代反应 |
| B | 向盛有溴水的两试管中分别加入一定量的乙烯和苯 | 两试管中的水层都逐渐褪色 | 乙烯和苯都与溴水发生了加成反应 |
| C | 向盛有少量无水乙醇的试管中,加入一小块新切的、用滤纸擦干表面煤油的金属钠 | 钠浮在无水乙醇表面,反应比钠在水中更剧烈 | 乙醇结构中羟基氢的活性比水中的强 |
| D | 将乙醇和浓硫酸共热至170℃后,将生成的气体通入酸性KMnO4溶液中 | KMnO4溶液褪色 | 证明乙烯能使KMnO4溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
19.下列微粒中,与甲烷分子具有相同的质子数和相同的电子数的是( )
| A. | H2O | B. | HCl | C. | NH4+ | D. | OH- |
16.下列实验现象不能说明相关结论的是( )
| A. | 加入氨水,产生白色沉淀,证明元溶液中存在Al3+ | |
| B. | 向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl溶解平衡正向移动 | |
| C. | 将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低 | |
| D. | 向饱和Ca(OH)2溶液中加入少量无水CaO,恢复原温度,溶液中Ca(OH)2的pH不变 |