题目内容
11.下列物质不属于酸性氧化物的是( )| A. | SO3 | B. | N2O5 | C. | Na2O | D. | CO2 |
分析 氧化物是由两种元素组成并且一种元素是氧元素的化合物,能和碱反应生成盐和水的氧化物属于酸性氧化物,能和酸反应生成盐和水的氧化物属于碱性氧化物.
解答 解:氧化钠能和酸反应生成盐和水,属于碱性氧化物,二氧化碳、SO3能和碱反应生成盐和水,属于酸性氧化物,N2O5既不是酸性氧化物也不是碱性氧化物,故选C.
点评 本题主要考查酸性氧化物、碱性氧化物的概念,解答时要根据氧化物性质进行分析、判断,从而得出正确的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.(1)CO2和CH4是两种重要的温室气体,通过CH4和CO2的反应,制造更高价值的化学品是目前的研究目标.250℃时,以镍合金为催化剂,发生如下反应:CO2(g)+CH4(g)?2CO(g)+2H2(g)
①此温度下该反应的平衡常数表达式K=$\frac{c(CO)^{2}×c({H}_{2})^{2}}{c(C{O}_{2})×c(C{H}_{4})}$.
②已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1
CO(g)+H2O(g)═CO2(g)+H2(g)△H=+2.8kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•mol-1
反应CO2(g)+CH4(g)?2CO(g)+2H2(g)的△H=+247.3kJ•mol-1kJ•mol-1;
(2)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H,
下表所列数据是该反应在不同温度下的化学平衡常数(K).
①根据表中数据可判断△H<0 (填“>”、“=”或“<”).
②300℃时,将2molCO、3molH2和2molCH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
③下列能说明上述反应达到化学平衡状态的标志是C
A.恒温恒容下,混合气体的密度不在变化
B.达平衡时,v(CO):v(H2):v(CH3OH)=1:2:1
C.达平衡时,CH3OH浓度不再变化
D.单位时间内生产nmolCO同时生成2nmolH2.
①此温度下该反应的平衡常数表达式K=$\frac{c(CO)^{2}×c({H}_{2})^{2}}{c(C{O}_{2})×c(C{H}_{4})}$.
②已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1
CO(g)+H2O(g)═CO2(g)+H2(g)△H=+2.8kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•mol-1
反应CO2(g)+CH4(g)?2CO(g)+2H2(g)的△H=+247.3kJ•mol-1kJ•mol-1;
(2)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H,
下表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②300℃时,将2molCO、3molH2和2molCH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
③下列能说明上述反应达到化学平衡状态的标志是C
A.恒温恒容下,混合气体的密度不在变化
B.达平衡时,v(CO):v(H2):v(CH3OH)=1:2:1
C.达平衡时,CH3OH浓度不再变化
D.单位时间内生产nmolCO同时生成2nmolH2.
19.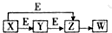 如图是某常见元素M的单质及其化合物间的转化关系图,其中X、Y、Z、W四种物质中均含有元素M,E是另一种单质,下列有关说法中不正确的是( )
如图是某常见元素M的单质及其化合物间的转化关系图,其中X、Y、Z、W四种物质中均含有元素M,E是另一种单质,下列有关说法中不正确的是( )
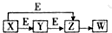 如图是某常见元素M的单质及其化合物间的转化关系图,其中X、Y、Z、W四种物质中均含有元素M,E是另一种单质,下列有关说法中不正确的是( )
如图是某常见元素M的单质及其化合物间的转化关系图,其中X、Y、Z、W四种物质中均含有元素M,E是另一种单质,下列有关说法中不正确的是( )| A. | W可能是硫酸 | B. | Y不可能是Mg | C. | X可能是钠 | D. | Z可能是CO2 |
16.下列说法正确的是( )
| A. | 高纯度的硅单质广泛用于制造光导纤维 | |
| B. | SiO2是酸性氧化物,不溶于任何酸 | |
| C. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| D. | 石灰石是生产玻璃和水泥的主要原料 |
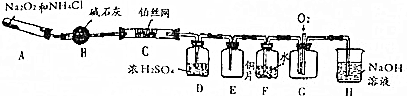
3.如图所示的装置可用于( )


| A. | 加热NaHCO3制CO2 | B. | 用Cu与稀硝酸反应制NO | ||
| C. | 用NH4Cl与浓NaOH溶液反应制NH3 | D. | 用锌与稀硫酸反应制H2 |
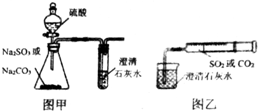 某同学用图甲所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2时可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象.经过思考分析,该同学改用图乙的装置,将气体收集在注射器中,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,结果都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生的现象明显比通入CO2快.
某同学用图甲所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2时可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象.经过思考分析,该同学改用图乙的装置,将气体收集在注射器中,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,结果都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生的现象明显比通入CO2快. 硼及其化合物的研究在无机化学的发展中占有独特的地位.
硼及其化合物的研究在无机化学的发展中占有独特的地位. H++B(OH)4-
H++B(OH)4-