题目内容
1.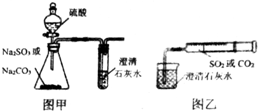 某同学用图甲所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2时可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象.经过思考分析,该同学改用图乙的装置,将气体收集在注射器中,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,结果都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生的现象明显比通入CO2快.
某同学用图甲所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2时可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象.经过思考分析,该同学改用图乙的装置,将气体收集在注射器中,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,结果都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生的现象明显比通入CO2快.(1)若锥形瓶内装的是亚硫酸钠,写出锥形瓶内发生反应的化学方程式:Na2SO3+H2SO4═Na2SO4+H2O+SO2↑.
(2)对比分析两组实验,你认为用图甲装置实验时,通入SO2不能出现浑浊的原因可能是反应时直接生成了酸式盐而看不到沉淀.写出此时试管内发生反应的总化学方程式:Ca(OH)2+2SO2═Ca(HSO3)2.
(3)用图乙装置实验时,以相同速率通入CO2或SO2,SO2产生浑浊再变澄清的现象比CO2快,其原因是SO2溶解度大,且对应的亚硫酸酸性比碳酸强,通入的SO2与石灰水反应快.
(4)用图甲进行SO2与澄清石灰水反应的实验时,为防止SO2污染空气,应用盛有过量浓烧碱溶液的容器吸收SO2,写出容器内发生反应的离子方程式:SO2+2OH-═SO32-+H2O.
分析 (1)亚硫酸钠与硫酸反应生成二氧化硫和水、硫酸钠;
(2)氢氧化钙溶液与足量二氧化硫反应生成可溶性亚硫酸钙和水;
(3)SO2溶解度大,且对应的亚硫酸酸性比碳酸强,通入的SO2与石灰水反应快,所以以相同速率通入CO2或SO2,SO2产生浑浊再变澄清的现象比CO2快;
(4)二氧化硫与氢氧化钠反应生成亚硫酸钠和水;
解答 解:(1)亚硫酸钠与硫酸反应生成二氧化硫和水、硫酸钠,方程式:Na2SO3+H2SO4═Na2SO4+H2O+SO2↑;
故答案为:Na2SO3+H2SO4═Na2SO4+H2O+SO2↑;
(2)氢氧化钙溶液与足量二氧化硫反应生成可溶性亚硫酸钙和水,离子方程式:Ca(OH)2+2SO2═Ca(HSO3)2;
故答案为:反应时直接生成了酸式盐而看不到沉淀;Ca(OH)2+2SO2═Ca(HSO3)2;
(3)SO2溶解度大,且对应的亚硫酸酸性比碳酸强,通入的SO2与石灰水反应快,所以以相同速率通入CO2或SO2,SO2产生浑浊再变澄清的现象比CO2快;
故答案为:SO2溶解度大,且对应的亚硫酸酸性比碳酸强,通入的SO2与石灰水反应快;
(4)二氧化硫与氢氧化钠反应生成亚硫酸钠和水,离子方程式:SO2+2OH-═SO32-+H2O;
故答案为:SO2+2OH-═SO32-+H2O;
点评 本题考查了二氧化硫的制备和性质,熟悉硫酸、二氧化硫的性质是解题关键,注意二氧化硫与二氧化碳与碱反应的相似性与区别,题目难度不大.

练习册系列答案
相关题目
12.如图a酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是由碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,下列说法不正确的是( )
有关数据如表所示:

有关数据如表所示:
| 温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |

| A. | 该电池的正极反应式为MnO2+eˉ+H+═MnOOH | |
| B. | 利用干电池,高温电解H2O-CO2混合气体制备H2和CO,如图b,则阴、阳两极生成的气体的物质的量之比是1:1 | |
| C. | 废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过重结晶方法分离 | |
| D. | 废电池糊状填充物加水处理后所得滤渣的主要成分是二氧化锰、碳粉和MnOOH,欲从中得到较纯的二氧化锰,可以采用加热的方法 |
16.下列鉴别物质的方法中,不正确的是( )
| A. | 用KSCN溶液鉴别FeCl2和FeCl3溶液 | |
| B. | 用澄清石灰水鉴别SO2和CO2 | |
| C. | 用焰色反应鉴别NaCl溶液和KCl洛液 | |
| D. | 用过量的NaOH溶液鉴别AlCl3溶液和MgCl2溶液 |
10.下列有关物质的应用:①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂②用明矾净水③草木灰与液态氮肥不能混合施用④用纯碱溶液洗涤蔬菜可适当去除农药残留⑤用TiCl4制备TiO2,其中与盐类的水解有关的是( )
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④⑤ |
11.下列物质不属于酸性氧化物的是( )
| A. | SO3 | B. | N2O5 | C. | Na2O | D. | CO2 |
 某校开展课外研究性学习:从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个过程如下,回答有关问题:
某校开展课外研究性学习:从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个过程如下,回答有关问题:
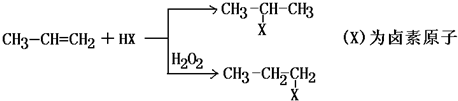

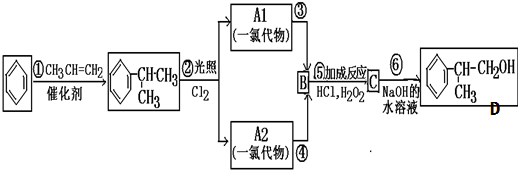
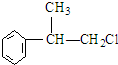 ,
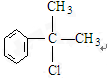
,
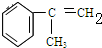 C的结构简式:
C的结构简式: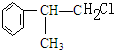 .
.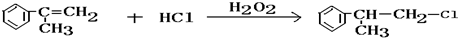 .
.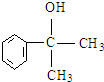 等.
等.