题目内容
20.在带活塞的圆筒内装入NO2气体,慢慢压缩,下列叙述正确的是( )| A. | 体积减半,压强为原来的2倍 | |
| B. | 体积减半,压强大于原来的2倍 | |
| C. | 体积减半,压强增大,但小于原来的2倍 | |
| D. | 体积减半,达到平衡后,n(NO2)变为原来的一半 |
分析 将NO2装入带活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡,慢慢压缩是增大压强,
A、体积减小一半,压强增大一倍,但平衡向气体体积减少的方向移动,最后达到平衡;
B、体积减小一半,压强增大一倍,但平衡向气体体积减少的方向移动,最后达到平衡;
C、压强增大平衡向气体体积减少的方向移动;
D、压强增大平衡向气体体积减少的方向移动,气体物质的量减小.
解答 解:将NO2装入带活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡后,慢慢压缩气体体积,压强增大平衡正向移动;
A、若体积减小一半,压强增大,平衡正向移动,压强小于原来的两倍,故A错误;
B、若体积减小一半,压强增大,平衡正向移动,压强小于原来的两倍,故B错误;
C、若体积减小一半,压强增大,V正增大,V逆增大,平衡正向移动,小于原来的两倍,故C正确;
D、体积减小一半,压强增大平衡向气体体积减少的方向移动,气体物质的量减小,二氧化氮物质的量减小,但不是原来的一半,故D错误;
故选C.
点评 本题考查了化学平衡的影响因素和应用,主要是恒压容器中化学平衡的变化,掌握分析方法和平衡移动原理是解题关键,题目难度中等.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
8.下列各组物质中互为同位素的是( )
| A. | $AlO_2^-$和${\;}_{18}^{40}Ar$ | B. | D和T | ||
| C. | H2O和H2O2 | D. | O3和O2 |
5. 工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )
工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )
 工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )
工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )| A. | 减小压强 | B. | 升高反应体系温度 | ||
| C. | 使用新型催化剂 | D. | 加入SO2 |
12.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 向NaAlO2溶液中通入过量CO2:2 AlO+CO2+3H2O═2Al(OH)3↓+CO | |
| D. | 以下有机物在碱性条件下水解的化学方程式: |
9.已知31g白磷变成红磷放出18.39kJ热量,下列两反应中:
P4(s)+5O2(g)═2P2O5(s)△H=Q1 kJ•mol-1
4P(红,s)+5O2(g)═2P2O5(s)△H=Q2kJ•mol-1
则下列说法中正确的是( )
P4(s)+5O2(g)═2P2O5(s)△H=Q1 kJ•mol-1
4P(红,s)+5O2(g)═2P2O5(s)△H=Q2kJ•mol-1
则下列说法中正确的是( )
| A. | Q1>Q2,白磷比红磷稳定 | B. | Q1>Q2,红磷比白磷稳定 | ||
| C. | Q1<Q2,白磷比红磷稳定 | D. | Q1<Q2,红磷比白磷稳定 |
10.下列说法正确的是( )
| A. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 同周期非金属氧化物对应水化物的酸性从左到右依次增强 | |
| D. | 第三周期元素的离子半径从左到右逐渐减小 |
 黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3.
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3.
 ;
; 、
、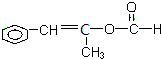 、
、 ;
; +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +NaCl+2H2O.
+NaCl+2H2O.