题目内容
10.某元素的同位素${\;}_{Z}^{A}$X,它的氯化物XCl2 11.1g溶于水制成溶液,加入1mol•L-1的AgNO3溶液200mL恰好完全反应.若这种同位素原子核内有20个中子,求:(1)Z值是20,A值是40.
(2)X元素在周期表中的位置是第四周期第ⅡA族.
(3)把X的单质放入水中其现象是有气泡产生,反应的化学方程式是Ca+2H2O═Ca(OH)2+H2↑.
分析 由Cl-+Ag+═AgCl↓计算XCl2的物质的量,再由M=$\frac{m}{M}$计算其摩尔质量,摩尔质量与相对分子质量的数值相等,原子的质量数为原子的近似相对原子质量,结合该原子原子核内有20个中子,根据质子数=质量数-中子数来计算原子的质子数,利用质子数确定元素在周期表中的位置,并利用质量守恒定律及X的性质来书写反应方程式.
解答 解:(1)由Cl-+Ag+═AgCl↓可知,n(Cl-)=n(Ag+)=0.2L×1mol/L=0.2mol,
n(XCl2)=$\frac{1}{2}$n(Cl-)=$\frac{1}{2}$×0.2mol=0.1mol,
则M(XCl2)=$\frac{11.1g}{0.1mol}$=111g/mol,
所以XCl2相对分子质量为111,
所以X的相对原子质量=111-35.5×2=40,即X的质量数为40,
质子数=质量数-中子数=40-20=20,即Z=20,A=40
故答案为:20;40;
(2)X为Ca,位于第四周期第ⅡA族,故答案为:第四周期第ⅡA族;
(3)X为Ca,性质活泼,与水反应生成氢气和氢氧化钙,反应的方程式为 Ca+2H2O═Ca(OH)2+H2↑,故答案为:有气泡产生;Ca+2H2O═Ca(OH)2+H2↑.
点评 本题考元素周期表的结构及应用,为高频考点,把握发生的离子反应及原子构成为解答的关键,注意分析与应用能力的考查,题目难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
20.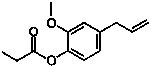 如图的有机物,则该有机物可发生的反应类型有( )
如图的有机物,则该有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚.
 如图的有机物,则该有机物可发生的反应类型有( )
如图的有机物,则该有机物可发生的反应类型有( )①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚.
| A. | ①②④⑤⑥ | B. | ①②③⑤⑦ | C. | ①②⑤⑥⑦ | D. | ①②④⑤⑦ |
1.下列有关说法正确的是( )
| A. | 氯水能导电,所以氯水属于电解质 | |
| B. | Al(OH)3既能溶于盐酸又能溶于NaOH溶液,属于两性氢氧化物 | |
| C. | 能电离产生H+的化合物一定是酸 | |
| D. | 饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 |
18.下列说法中正确的是( )
| A. | 氢原子光谱是原子的所有光谱中最简单的光谱之一 | |
| B. | “量子化”就是不连续的意思,微观粒子运动均有此特点 | |
| C. | 玻尔理论不但成功地解释了氢原子光谱,而且还推广到其他原子光谱 | |
| D. | 原子中的电子在具有确定半径的圆周轨道上像火车一样高速运转着 |
5.下列说法正确的是( )
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 共价化合物中只有极性键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 非极性键只存在于单质分子中 |
15.下列表示对应化学反应的离子方程式正确的是( )
| A. | NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ | |
| B. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将少量SO2通入冷氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O |
2.A和B两元素能形成AB2 型离子化合物,则A和B的原子序数可能是( )
| A. | 6和8 | B. | 11和6 | C. | 20和8 | D. | 20和17 |
19.将0.1mol的镁、铝混合物完全溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,当沉淀达到最大值时所加入NaOH溶液的体积为( )
| A. | 100mL | B. | 200mL | C. | 300mL | D. | 400mL |
20.在带活塞的圆筒内装入NO2气体,慢慢压缩,下列叙述正确的是( )
| A. | 体积减半,压强为原来的2倍 | |
| B. | 体积减半,压强大于原来的2倍 | |
| C. | 体积减半,压强增大,但小于原来的2倍 | |
| D. | 体积减半,达到平衡后,n(NO2)变为原来的一半 |