题目内容
某研究性学习小组讨论甲、乙、丙、丁四种实验装置的有关用法,其中正确的是( )


| A、甲装置:可用来除去CO气体中的CO2气体 |
| B、乙装置:可用来验证NaHCO3和Na2CO3的热稳定性 |
| C、丙装置:可用来实验室制备乙酸乙酯 |
| D、丁装置:可用来比较HCl、H2CO3和H2SiO3的酸性强弱 |
考点:化学实验方案的评价
专题:
分析:A.洗气时导管长进短出;
B.碳酸氢钠不稳定,加热分解,而碳酸钠稳定;
C.乙酸与乙醇在浓硫酸作用下反应生成乙酸乙酯,饱和碳酸钠可除杂乙酸、乙醇,与碳酸钠分层;
D.图中发生强酸制取弱酸的反应,且盐酸易挥发.
B.碳酸氢钠不稳定,加热分解,而碳酸钠稳定;
C.乙酸与乙醇在浓硫酸作用下反应生成乙酸乙酯,饱和碳酸钠可除杂乙酸、乙醇,与碳酸钠分层;
D.图中发生强酸制取弱酸的反应,且盐酸易挥发.
解答:
解:A.洗气时导管长进短出,则图中进气导管应长导管进入,故A错误;
B.碳酸氢钠不稳定,加热分解,而碳酸钠稳定,则小试管中应为碳酸氢钠,故B错误;
C.乙酸与乙醇在浓硫酸作用下反应生成乙酸乙酯,饱和碳酸钠可除杂乙酸、乙醇,与碳酸钠分层,图中装置可制备乙酸乙酯,故C正确;
D.图中发生强酸制取弱酸的反应,且盐酸易挥发,则图中装置不能比较H2CO3和H2SiO3酸性,故D错误;
故选C.
B.碳酸氢钠不稳定,加热分解,而碳酸钠稳定,则小试管中应为碳酸氢钠,故B错误;
C.乙酸与乙醇在浓硫酸作用下反应生成乙酸乙酯,饱和碳酸钠可除杂乙酸、乙醇,与碳酸钠分层,图中装置可制备乙酸乙酯,故C正确;
D.图中发生强酸制取弱酸的反应,且盐酸易挥发,则图中装置不能比较H2CO3和H2SiO3酸性,故D错误;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、物质的性质、物质的制备、酸性比较及实验基本操作等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 下表中各组物质之间不能通过一步反应实现如图的是( )
下表中各组物质之间不能通过一步反应实现如图的是( ) | 甲 | 乙 | 丙 | |
| A | NaHCO3 | Na2CO3 | NaCl |
| B | SiO2 | HSiO3 | Na2SiO3 |
| C | Cl2 | HCl | CuCl2 |
| D | AlCl3 | Al(OH)3 | Al2O3 |
| A、A | B、B | C、C | D、D |
如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是其中的五种元素.下列说法不正确的是( )


| A、原子半径:W>Z |
| B、最高价氧化物的水化物的酸性:R>W |
| C、气态氢化物的稳定性:X>W |
| D、单质与水(或酸)反应的剧烈程度:Y>Z |
可能存在的第119号未知元素,有人称为“类钫”,根据周期表结构及元素性质变化趋势,有关“类钫”的预测,说法不正确的是( )
| A、“类钫”在化合物中是+1价 |
| B、“类钫”具有放射性 |
| C、“类钫”单质的密度大于l g?cm-3 |
| D、“类钫”单质有较高的熔点 |
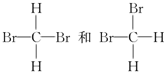 E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和





 元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题: