题目内容
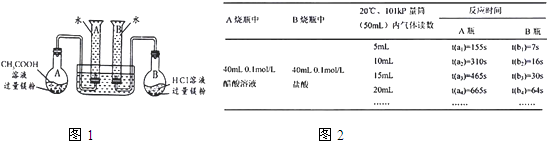
锌与100mL1mol×L-1HCl反应的实验中,若设想向溶液中加入少量的①醋酸钠,或②溴化铜,或③醋酸铜(均为可溶性),并测定生成氢气的速率(mL/min),预计三种方案的速率大小是( )
A.①>③>② B.③>②>① C.②>③>① D.①>②>③
答案:C
解析:
解析:
③中形成原电池的同时生成CH3COOH,降低c(H+),而②中形成原电池但不降低c(H+),故选C。
|

练习册系列答案
相关题目
下列事实不能用电化学原理解释的是( )
| A、镀锌铁片比镀锡铁片更耐腐蚀 | B、远洋海轮的尾部装上一定数量的锌板 | C、常温条件下,在空气中铝不易被腐蚀 | D、用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
下列事实不能用电化学理论解释的是( )
| A、土壤内的输水钢管总是通过导线连接一镁块,并定时更换镁 | B、铝片可以露置在空气中存放 | C、轮船吃水线以下的船壳上装有一定数量的锌块 | D、纯锌与稀硫酸反应制取氢气时,滴入少量的硫酸铜溶液使反应速率加快 |
下列依据相关实验得出的结论正确的是( )
| A、加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 | B、纤维素的水解产物能够发生银镜反应,说明纤维素是一种还原性糖 | C、向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀,说明该溶液中含有SO42- | D、等物质的量浓度的H3PO4溶液的pH比H2SO4溶液大,说明硫比磷的非金属性强 |