题目内容
下列说法不正确的是( )
| A、NaClO、NaClO2、KClO3、NaClO4中Cl的化合价依次升高 |
| B、C与CuO高温共热,C的氧化产物只能是CO2 |
| C、H2SO4由分子构成,溶于水离解成H+和SO42- |
| D、Al与Fe2O3高温反应生成Al2O3与Fe,属于置换反应 |
考点:根据化学式判断化合价,电解质在水溶液中的电离,铝的化学性质,铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:A.NaClO中Cl为+1价、NaClO2中Cl为+3价、KClO3中Cl为+5价、NaClO4中Cl为+7价;
B.C与CuO高温共热,C的氧化产物可能是CO2或CO;
C.H2SO4是共价化合物,由分子构成,溶于水电离出H+和SO42-;
D.置换反应:指一种单质和一种化合物生成另一种单质和另一种化合物的反应.
B.C与CuO高温共热,C的氧化产物可能是CO2或CO;
C.H2SO4是共价化合物,由分子构成,溶于水电离出H+和SO42-;
D.置换反应:指一种单质和一种化合物生成另一种单质和另一种化合物的反应.
解答:
解:A.NaClO中Cl为+1价、NaClO2中Cl为+3价、KClO3中Cl为+5价、NaClO4中Cl为+7价,故化合价依次升高,故A正确;
B.C与CuO高温共热,C的氧化产物可能是CO2或CO,故B错误;
C.H2SO4是共价化合物,由分子构成,溶于水电离出H+和SO42-,故C正确;
D.一种单质和一种化合物生成另一种单质和另一种化合物,属于置换反应,故D正确;
故选B.
B.C与CuO高温共热,C的氧化产物可能是CO2或CO,故B错误;
C.H2SO4是共价化合物,由分子构成,溶于水电离出H+和SO42-,故C正确;
D.一种单质和一种化合物生成另一种单质和另一种化合物,属于置换反应,故D正确;
故选B.
点评:本题考查元素化合价的判断、氧化还原反应、共价化合物和置换反应,难度不大.要注意基础知识的积累.

练习册系列答案
相关题目
除去镁粉中含有的杂质铝粉可选用的溶液是( )
| A、硫酸 | B、氢氧化钠 |
| C、氨水 | D、氯化铜 |
金刚石、石墨物理性质不同的原因是( )
| A、组成的元素不同 |
| B、金刚石是单质,石墨是化合物 |
| C、碳原子结构不同 |
| D、碳原子的排列方式不同 |
实验操作的规范是实验的基本要求,下列实验操作正确的是( )
A、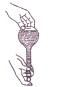 检验容量瓶是否漏水 |
B、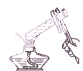 给溶液加热 |
C、 滴加液体 |
D、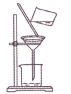 过滤 |
下列说法正确的是( )
| A、丙烷是直链烃,所以分子中3个碳原子也在一条直线上 |
| B、丙烯所有原子均在同一平面上 |
C、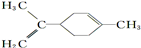 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D、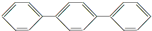 至少有16个原子共平面 至少有16个原子共平面 |
12.8g铜跟适量的浓硝酸反应,铜完全作用后,共收集到气体5.6L(标准状况),反应消耗HNO3的物质的量可能是( )
| A、0.25mol |
| B、1.0mol |
| C、0.65mol |
| D、0.5mol |
氯化溴(BrCl)和Br2、Cl2具有相似的性质,下列有关氯化溴性质的判断中错误的是( )
| A、在CCl4中的溶解性BrCl<Br2 |
| B、BrCl氧化性比Br2强,比Cl2弱 |
| C、沸点BrCl>Br2 |
| D、常温下BrCl可与NaOH溶液反应生成NaCl和NaBrO |
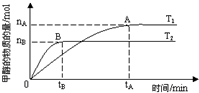 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题: