题目内容
|
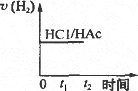
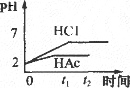
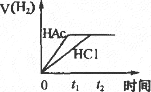
向体积均为1 L,pH均等于2的盐酸和醋酸中,分别投入0.28 g Fe,则下图中的曲线符合反应事实的是 | |
A. |
|
B. |
|
C. |
|
D. |
|
答案:BC
解析:
解析:
|
根据题中所给信息首先判断出盐酸和醋酸的c(H+)一样.其中n(CH3COOH)>n(HCl)=0.01 mol.0.005 mol Fe恰好与盐酸完全反应.然后对照图像一一判断.A项中开始时,由于H+浓度相等,则两者速度一样,但随着反应的进行,醋酸中c(H+)大于盐酸中c(H+),故醋酸中产生H2的速度快,A错;B项中开始时pH都等于2,随着反应的进行,盐酸的pH增大的快,B正确;C选项中由于c(CH3COOH)>c(HCl),所以醋酸放出氢气快,反应时间短,且由于Fe不足量,所以最后两者放出氢气一样多,C对;D选项中,醋酸中c(H+)应先缓慢减小,当Fe反应完后c(H+)不再变化,D错.故应选BC.此题是一道综合性比较强的好题,从不同角度考查了HCl和CH3COOH与Fe反应中浓度的变化,放出H2的速度的变化、pH的变化等各种实际问题,能提高学生从多角度思考问题的能力. |

练习册系列答案
相关题目

 (2009?丹东模拟)甲醇可以与水蒸气反应生成氢气,反应方程式如下:
(2009?丹东模拟)甲醇可以与水蒸气反应生成氢气,反应方程式如下:
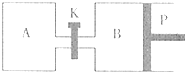
 (08浙江金丽衢十二校联考)如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)
(08浙江金丽衢十二校联考)如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)
 CO2(g)+3H2(g) ΔH>0
CO2(g)+3H2(g) ΔH>0 