题目内容
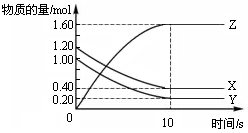
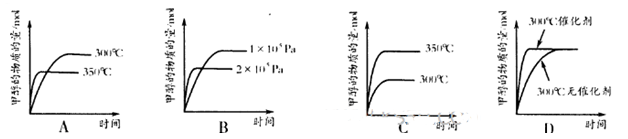
在恒温条件下,将气体X、Y充入2 L密闭容器中反应生成气体Z。若各气体的物质的量随时间变化曲线如图所示,下列描述正确的是

| A.前10s内 v(X)=0.08mol·L-1·s-1 |
| B.该反应的平衡常数K= 4 |
| C.平衡时X、Y的转化率相同 |
| D.达到平衡后,将容器体积扩大为 4 L,平衡向逆反应方向移动 |
B
试题分析:A.由物质的量与时间的关系曲线可知在前10s内 v(X)=(1.20-0.40)÷2L÷10s="0.04mol/(" L·s)。错误。B.从反应开始至达到平衡各物质的物质的量的变化是:X:减少0.80mol;Y减少0.80mol;Z增加1.60mol.后来随着时间的推移,各种物质的物质的量不变,反应达到平衡。因此反应方程式为X(g)+Y(g)
 2Z(g)。在平衡时,各种物质的浓度分别是X:0.4mol/L;Y:0.40mol/L;Z:0.80mol/L。因此该反应的平衡常数K=0.802 ÷(0.4×0.4)=4.正确。 C.当反应达到平衡时X的转化率="0.8÷1.2=1/3;" 的转化率=0.8÷1=4/5,并不相同,错误。D.达到平衡后,将容器体积扩大为 4 L,即减小压强。由于该反应是反应前后气体体积相等的反应,所以减小压强,化学平衡不发生移动。错误。
2Z(g)。在平衡时,各种物质的浓度分别是X:0.4mol/L;Y:0.40mol/L;Z:0.80mol/L。因此该反应的平衡常数K=0.802 ÷(0.4×0.4)=4.正确。 C.当反应达到平衡时X的转化率="0.8÷1.2=1/3;" 的转化率=0.8÷1=4/5,并不相同,错误。D.达到平衡后,将容器体积扩大为 4 L,即减小压强。由于该反应是反应前后气体体积相等的反应,所以减小压强,化学平衡不发生移动。错误。
练习册系列答案
相关题目
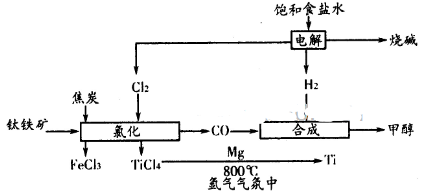
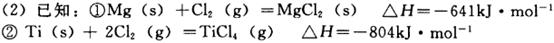
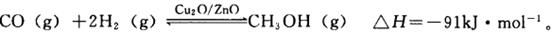
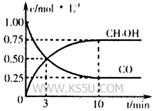
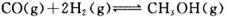 的化学平衡常
的化学平衡常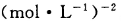 。
。
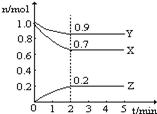
 2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)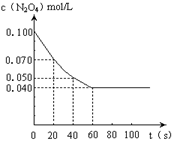
 p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为 2NH3(g) ΔH<0,反应过程如图:下列说法正确的是
2NH3(g) ΔH<0,反应过程如图:下列说法正确的是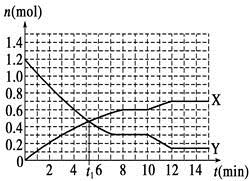
 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是