题目内容
1.含1.806×1023个分子的N2,在标准状况下的体积是6.72L.分析 根据n=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$计算.
解答 解:n(N2)=$\frac{1.806×1{0}^{23}}{6.02×1{0}^{23}/mol}$=0.3mol,V=0.3mol×22.4L/mol=6.72L,
故答案为:6.72.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
11.下列化学实验操作或事故处理方法不正确的是( )
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 | |
| C. | 酒精灯着火时可用湿布扑灭 | |
| D. | 蒸馏时,温度计水银球应浸没在液体中 |
12.对于反应2SO2+O2?2SO3,下列说法正确的是( )
| A. | 工业上常使用过量的空气,目的是为了使SO2的转化率达100% | |
| B. | 工业上选用V2O5作该反应的催化剂,目的是为了加快化学反应速率 | |
| C. | 工业上常选用常压,原因是增大压强不能改变该反应的化学反应速率 | |
| D. | 升高温度可以加快反应速率,所以在工业生产中该反应温度越高越好 |
6.下列物质分类中,前者包含后者的是( )
| A. | 酸性氧化物 非金属氧化物 | B. | 溶液 胶体 | ||
| C. | 化合物 电解质 | D. | 有机物 分散系 |
13.常用两种方法制备氯化物:①金属与氯气直接化合;②金属与盐酸反应.用上述两种方法都可制得的氯化物是( )
| A. | CuCl2 | B. | FeCl2 | C. | FeCl3 | D. | AlCl3 |
10. 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的物质的量浓度是3.5×10-3mol•L-1;平衡时,NO的转化率为65%;
(2)已知该反应反应物的总能量大于生成物的总能量,则该反应是放热(填“放热”或“吸热”)反应.
(3)用O2表示从0-2s内该反应的平均速率v(O2)=1.5×10-3mol•L-1•s-1.
(4)如图中表示c(NO2)随时间的变化曲线是b.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)已知该反应反应物的总能量大于生成物的总能量,则该反应是放热(填“放热”或“吸热”)反应.
(3)用O2表示从0-2s内该反应的平均速率v(O2)=1.5×10-3mol•L-1•s-1.
(4)如图中表示c(NO2)随时间的变化曲线是b.
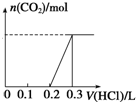 100mL 1mol•L-1烧碱溶液中通入一定量CO2充分反应后,将溶液在低温下蒸干得到白色固体X,X的组成可能有四种情况,
100mL 1mol•L-1烧碱溶液中通入一定量CO2充分反应后,将溶液在低温下蒸干得到白色固体X,X的组成可能有四种情况,

