题目内容
17.你认为某同学的下列想法正确的是( )| A. | 聚合反应符合“绿色化学工艺”要求,即原子利用率100% | |
| B. | 用聚乙烯塑料代替聚乳酸塑料可明显减少白色污染 | |
| C. | 装修材料中常挥发出有害气体甲醛等,入住新居前放几盆清水便可 | |
| D. | 乙醇、双氧水在医疗上常用作杀菌消毒剂 |
分析 A.依据缩聚反应特点:反应产物除了目标产物外还有小分子化合物解答;
B.聚乙烯塑料难降解,聚乳酸塑料能降解;
C.装修材料中常挥发出有害气体有些不溶于水,例如苯及其同系物;
D.乙醇、双氧水都能使蛋白质变性.
解答 解:A.依据缩聚反应特点:反应产物除了目标产物外还有小分子化合物,原子利用率1小于00%,故A错误;
B.用聚乳酸塑料代替聚聚乙烯塑料可明显减少白色污染,故B错误;
C.装修材料中常挥发出有害气体有些不溶于水,例如苯及其同系物,所以入住新居前放几盆清水便可不能完全除去有毒气体,故C错误;
D.乙醇、双氧水都能使蛋白质变性,在医疗上常用作杀菌消毒剂,故D正确;
故选:D.
点评 本题考查了化学与生产生活的关系,侧重考查生活中常见的环境污染与治理,明确绿色化学概念、及常见污染的治理是解题关键,题目难度中等.

练习册系列答案
相关题目
7.下列物质的分子中既有σ键,又有π键,并含有非极性键的是( )
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2.
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2.
| A. | ①②③ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
8.下列物质中,属于天然高分子化合物的是( )
| A. | 聚乙烯 | B. | 蔗糖 | C. | 淀粉 | D. | 麦芽糖 |
5.等物质的量的CH4、C2H4、C2H2,分别在足量的氧气中充分燃烧,以下说法正确的是( )
| A. | C2H2含碳量最高,燃烧生成的CO2最多 | |
| B. | C2H4燃烧生成水与CO2的物质的量相等 | |
| C. | CH4含氢量最高,燃烧生成水最多 | |
| D. | CH4、C2H4燃烧生成水的质量不相同,消耗氧气不同 |
12.肉桂酸是一种香料,具有很好的保香作用,通常作为配香原料,可使主香料的香气更加清香.实验室制备肉桂酸的化学方程式为:

主要试剂及其物理性质
密度:常压,25℃测定
主要实验步骤和装置如下:

Ⅰ合成:按图1连接仪器,加入5mL苯甲醛、14mL乙酸酐和7.02g无水碳酸钾.在140~170℃,将此混合物回流45min.
Ⅱ分离与提纯:
①将上述合成的产品冷却后边搅拌边加入40ml水浸泡5分钟,并用水蒸气蒸馏,从混合物中除去未反应的苯甲醛,得到粗产品
②将上述粗产品冷却后加入40ml 10%的氢氧化钠水溶液,再加90ml水,加热活性炭脱色,趁热过滤、冷却;
③将1:1的盐酸在搅拌下加入到肉桂酸盐溶液中,至溶液呈酸性,经冷却、减压过滤、洗涤、干燥等操作得到较纯净的肉桂酸;
水蒸气蒸馏:使有机物可在较低的温度下从混合物中蒸馏出来,可以避免在常压下蒸馏时所造成的损失,提高分离提纯的效率.同时在操作和装置方面也较减压蒸馏简便一些,所以水蒸气蒸馏可以应用于分离和提纯有机物.
回答下列问题:
(1)合成肉桂酸的实验需在无水条件下进行,实验前仪器必须干燥.实验中为控制温度在140~170℃需在BD中加热(请从下列选项中选择).
A.水 B.甘油(沸点290℃) C.砂子 D.植物油(沸点230~325℃)反应刚开始时,会有乙酸酐(有毒)挥发,所以该实验应在通风橱或通风处中进行操作.
(2)图2中装置a的作用是产生水蒸气,装置b中长玻璃导管要伸入混合物中的原因是使混合物与水蒸气充分接触,有利于提纯肉桂酸,水蒸气蒸馏后产品在三颈烧瓶(填仪器名称)
(3)趁热过滤的目的防止肉桂酸钠结晶而析出堵塞漏斗,方法:用热过滤漏斗或采取保温措施.
(4)加入1:1的盐酸的目的是使肉桂酸盐转化为肉桂酸,析出的肉桂酸晶体通过减压过滤与母液分离.下列说法正确的是ACD.
A.选择减压过滤是因为过滤速度快而且能得到较干燥的晶体
B.放入比布氏漏斗内径小的滤纸后,直接用倾析法转移溶液和沉淀,再迅速开大水龙头抽滤
C.洗涤产物时,先关小水龙头,用冷水缓慢淋洗
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,再关水龙头
(5)5mL苯甲醛、14mL乙酸酐和7.02g无水碳酸钾充分反应得到肉桂酸实际3.1g,则产率是41.9%(保留3位有效数字).

主要试剂及其物理性质
| 名称 | 分子量 | 性状 | 密度g/cm3 | 熔点℃ | 沸点℃ | 溶解度:克/100ml溶剂 | ||
| 水 | 醇 | 醚 | ||||||
| 苯甲醛 | 106 | 无色液体 | 1.06 | -26 | 178-179 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 无色液体 | 1.082 | -73 | 138-140 | 12 | 溶 | 不溶 |
| 肉桂酸 | 148 | 无色结晶 | 1.248 | 133-134 | 300 | 0.04 | 24 | 溶 |
主要实验步骤和装置如下:

Ⅰ合成:按图1连接仪器,加入5mL苯甲醛、14mL乙酸酐和7.02g无水碳酸钾.在140~170℃,将此混合物回流45min.
Ⅱ分离与提纯:
①将上述合成的产品冷却后边搅拌边加入40ml水浸泡5分钟,并用水蒸气蒸馏,从混合物中除去未反应的苯甲醛,得到粗产品
②将上述粗产品冷却后加入40ml 10%的氢氧化钠水溶液,再加90ml水,加热活性炭脱色,趁热过滤、冷却;
③将1:1的盐酸在搅拌下加入到肉桂酸盐溶液中,至溶液呈酸性,经冷却、减压过滤、洗涤、干燥等操作得到较纯净的肉桂酸;
水蒸气蒸馏:使有机物可在较低的温度下从混合物中蒸馏出来,可以避免在常压下蒸馏时所造成的损失,提高分离提纯的效率.同时在操作和装置方面也较减压蒸馏简便一些,所以水蒸气蒸馏可以应用于分离和提纯有机物.
回答下列问题:
(1)合成肉桂酸的实验需在无水条件下进行,实验前仪器必须干燥.实验中为控制温度在140~170℃需在BD中加热(请从下列选项中选择).
A.水 B.甘油(沸点290℃) C.砂子 D.植物油(沸点230~325℃)反应刚开始时,会有乙酸酐(有毒)挥发,所以该实验应在通风橱或通风处中进行操作.
(2)图2中装置a的作用是产生水蒸气,装置b中长玻璃导管要伸入混合物中的原因是使混合物与水蒸气充分接触,有利于提纯肉桂酸,水蒸气蒸馏后产品在三颈烧瓶(填仪器名称)
(3)趁热过滤的目的防止肉桂酸钠结晶而析出堵塞漏斗,方法:用热过滤漏斗或采取保温措施.
(4)加入1:1的盐酸的目的是使肉桂酸盐转化为肉桂酸,析出的肉桂酸晶体通过减压过滤与母液分离.下列说法正确的是ACD.
A.选择减压过滤是因为过滤速度快而且能得到较干燥的晶体
B.放入比布氏漏斗内径小的滤纸后,直接用倾析法转移溶液和沉淀,再迅速开大水龙头抽滤
C.洗涤产物时,先关小水龙头,用冷水缓慢淋洗
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,再关水龙头
(5)5mL苯甲醛、14mL乙酸酐和7.02g无水碳酸钾充分反应得到肉桂酸实际3.1g,则产率是41.9%(保留3位有效数字).
2.某同学写出下列烷烃的名称中,不正确的是( )
| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 3-甲基-3-乙基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
9.下表列出了前20号元素中的某些元素性质的有关数据:
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是②(填写编号).
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)PCl3、CCl4.某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期ⅥA族.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是②(填写编号).
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)PCl3、CCl4.某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期ⅥA族.
6.阿魏酸化学名称为4-羟基-3-甲氧基肉桂酸,可以做医药、保健品、化妆品原料和食品添加剂,结构简式为 ,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( )
,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( )
 ,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( )
,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( ) | 选项 | 试剂 | 现象 | 结论 |
| A | 氧化铁溶液 | 溶液变蓝色 | 它含有酚羟基 |
| B | 银氨溶液 | 产生银镜 | 它含有醛基 |
| C | 碳酸氢钠溶液 | 产生气泡 | 它含有羧基 |
| D | 溴水 | 溶液褪色 | 它含有碳碳双键 |
| A. | A | B. | B | C. | C | D. | D |
9.某科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)═2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是( )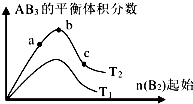

| A. | 反应速率a>b>c | |
| B. | 达到平衡时 A2的转化率大小为:b>a>c | |
| C. | 若T2>T1,则正反应一定是吸热反应 | |
| D. | 达到平衡时,AB3的物质的量大小为:b>c>a |