题目内容
16.下列离子方程式的书写中,正确的是( )| A. | 硫酸氢钾和氢氧化钡按等物质的量在溶液中反应:Ba2++OH-+H++SO42-=BaSO4↓+2H2O | |
| B. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++CO2↑+2H2O | |
| C. | 过量二氧化碳跟苛性钾反应; CO2+2OH-=CO32-+H2O | |
| D. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
分析 A.二者等物质的量反应时,离子方程式按照硫酸氢钾的化学式书写;
B.醋酸为弱酸,不能拆开;
C.二氧化碳过量,反应生成碳酸氢钾;
D.电荷不守恒.
解答 解:A.碳酸氢钾和氢氧化钡按等物质的量在溶液中反应的离子方程式为:H++SO42-+Ba2++OH-=BaSO4↓+H2O,故A正确;
B.醋酸为弱酸,不能拆,写成化学式,故B错误;
C.过量二氧化碳跟苛性钾反应生成碳酸氢钾,正确的离子方程式为:CO2+OH-=HCO3-,故C错误;
D.钠跟水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故D错误;
故选:A.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.铜与浓硝酸反应,产生气体通过排水法可以收集到的气体是( )
| A. | NO | B. | NO2 | C. | N2 | D. | N2O |
4.下列各组有机物,无论它们以何种比例混和,只要总质量一定,则在完全燃烧时,消耗氧气的量为一定值的是( )
| A. | C2H6和C3H8 | B. | C4H10和C6H6 | C. | CH2O和 C2H4O2 | D. | C3H6和C3H8O |
11.${\;}_{6}^{13}$C-NMR(核磁共振)可用于含碳化合物的结构分析,${\;}_{6}^{13}$C表示的碳原子( )
| A. | 核外有13个电子,核内有13个质子 | |
| B. | 核内有6个质子,核外有7个电子 | |
| C. | 质量数为13,原子序数为6,核内有7个质子 | |
| D. | 质量数为13,原子序数为6,核内有7个中子 |
8.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常温下,0.1molH2O2中含有极性共价键的数目为0.1NA | |
| B. | 电解饱和食盐水时,当阴极产生22.4LH2时,电路中转移的电子数为2NA | |
| C. | 100mL12mol•L-1的浓HNO3与过量Cu反应转移电子的数目为0.6NA | |
| D. | 标准状况下,11.2L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
6.下列属于吸热反应的是( )
| A. | 镁的燃烧反应 | B. | 盐酸与氢氧化钠的反应 | ||
| C. | 水的分解反应 | D. | 铝与氧化铁的铝热反应 |
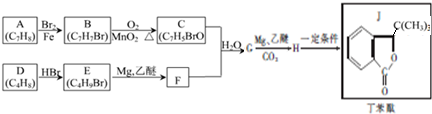
 某研究小组为了探究甲烷和氯气反应的情况,请填空:
某研究小组为了探究甲烷和氯气反应的情况,请填空:
 .
. .
. ②
② 中氯原子在水溶液中不水解,写出2-氯甲苯(
中氯原子在水溶液中不水解,写出2-氯甲苯( )经两步反应合成A的化学方程式.
)经两步反应合成A的化学方程式. ,
, 合成A时产生的有机副产物可能是
合成A时产生的有机副产物可能是 、
、 .
.
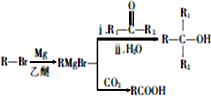
 .
.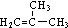 +HBr→(CH3)3CBr.
+HBr→(CH3)3CBr.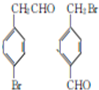 .
. )
) .
.