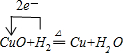题目内容
19.下列关于胶体的叙述正确的是( )| A. | 胶体区别于其他分散系的本质特征是丁达尔现象 | |
| B. | 将饱和FeCl3溶液逐滴加入NaOH溶液中可制备Fe(OH)3胶体 | |
| C. | Al(OH)3胶体能使水中的悬浮颗粒沉降,达到净水的目的 | |
| D. | 豆浆、蔗糖溶液均属于胶体 |
分析 A.胶体区别于其他分散系最本质的特征是胶体是分散质粒子直径的大小;
B.饱和FeCl3溶液和NaOH溶液反应生成氢氧化铁沉淀;
C.胶体具有较大的表面积,能吸附水中悬浮的固体颗粒;
D.蔗糖溶液属于溶液.
解答 解:A.胶体区别于其他分散系最本质的特征是胶体是分散质粒子直径10-9-10-7m之间,故A错误;
B.反应生成沉淀,而实验室制备氢氧化铁胶体是把饱和氯化铁溶液滴入沸水中加热到呈红褐色液体,即得到氢氧化铁胶体,故B错误;
C.Al(OH)3胶体具有较大的表面积,能够使水中悬浮的固体颗粒沉降,达到净水目的,故C正确;
D.豆浆属于胶体,蔗糖溶液属于溶液,故D错误.
故选C.
点评 本题考查胶体的特性以及溶液和胶体的本质区别,熟悉胶体的性质是解答的关键,题目较简单.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
10.硅及其化合物的开发由来已久,在现代生活中有广泛应用.回答下列问题.
(1)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
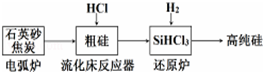
①还原炉中发生主要反应的化学方程式为SiHCl3+H2$\frac{\underline{\;高温\;}}{\;}$Si+3HCl,该工艺中可循环使用的物质为HCl和H2(填化学式).用石英砂和焦炭在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和精馏.
③SiHCl3极易水解,其完全水解的化学方程式为SiHCl3+3H2O═H2SiO3+H2↑+3HCl↑.
(2)氮化硅(Si3N4)是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取.粉末状Si3N4遇空气和水都不稳定,但将粉末状的Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中进行热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到遇水不稳定的Mg3N2.
①由SiCl4和NH3反应制取Si3N4的化学方程式为3SiCl4+4NH3$\frac{\underline{\;高温\;}}{\;}$Si3N4+12HCl.
②四氯化硅和氮气在氢气气氛保护下,加强热发生反应,使生成的Si3N4沉积在石墨表面可得较高纯度的氮化硅,该反应的化学方程式为3SiCl4+2N2+6H2$\frac{\underline{\;高温\;}}{\;}$Si3N4+12HCl.
③Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中进行热处理的过程中,除生成Mg3N2外,还可能生成SiO2物质(填化学式).热处理后除去MgO和Mg3N2的方法是加足量稀盐酸过滤.
(1)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:

| 发生的主要反应 | |
| 电弧炉 | SiO2+2C$\frac{\underline{\;1600-1800℃\;}}{\;}$si+2CO |
| 流化床反应器 | Si+3HCl$\frac{\underline{\;250-300\;}}{\;}$SiHCl3+H2 |
| 还原炉 |
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和精馏.
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/°C | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
(2)氮化硅(Si3N4)是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取.粉末状Si3N4遇空气和水都不稳定,但将粉末状的Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中进行热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到遇水不稳定的Mg3N2.
①由SiCl4和NH3反应制取Si3N4的化学方程式为3SiCl4+4NH3$\frac{\underline{\;高温\;}}{\;}$Si3N4+12HCl.
②四氯化硅和氮气在氢气气氛保护下,加强热发生反应,使生成的Si3N4沉积在石墨表面可得较高纯度的氮化硅,该反应的化学方程式为3SiCl4+2N2+6H2$\frac{\underline{\;高温\;}}{\;}$Si3N4+12HCl.
③Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中进行热处理的过程中,除生成Mg3N2外,还可能生成SiO2物质(填化学式).热处理后除去MgO和Mg3N2的方法是加足量稀盐酸过滤.
7.锌跟盐酸反应的离子方程式是:Zn+2H+═Zn2++H2↑.在如表所列的条件下,反应速率最大的是( )
| 选项 | 温度/K | 锌 | c(Zn2+)/mol/L | c(H+)/mol/L | 另加溶液 |
| A | 281 | 锌块 | 0.1 | 3 | |
| B | 308 | 锌粉 | 0.2 | 3 | 少量氯化铜 |
| C | 281 | 锌块 | 0.1 | 2 | |
| D | 308 | 锌粉 | 0.1 | 3 | 少量氯化钡 |
| A. | A | B. | B | C. | C | D. | D |
14.下列各组离子在水溶液中能够大量共存的是( )
| A. | H+、CO32-、NO3- | B. | Cu2+、Cl-、OH- | C. | Na+、Cl-、HCO3- | D. | Ag+、K+、Cl- |
4.下列说法正确的是( )
| A. | 硫酸钡难溶于水,其水溶液导电能力极弱,所以硫酸钡不是电解质 | |
| B. | CO2溶于水得到的溶液能导电,所以CO2是电解质 | |
| C. | 酸、碱和盐类都属于电解质,其他物质都是非电解质 | |
| D. | 电解质与非电解质的本质区别是在水溶液或熔化状态下能否电离 |
11.下列物质中,可用作净水剂的是( )
| A. | 纯碱 | B. | 明矾 | C. | 蔗糖 | D. | 火碱 |
8.设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下,50g SO2和CO2的混合气体中可能含有2NA个氧原子 | |
| B. | I mol Cl2与足量的铁反应,转移的电子数为3NA | |
| C. | 1 L0.1 mol•L-1氨水含有0.l NA个OH- | |
| D. | I mol乙醇中含有C-H键的数目为6NA |