题目内容
纯度测定是化学实验中经常碰到的问题,结合实验原理和实验用品,纯度测定可有多种选择。(1)工业纯碱中含少量NaCl,若实验室只提供盐酸、天平、蒸发皿、玻璃棒、铁架台(带铁夹、铁圈),请设计一个方案,测定纯碱样品的纯度。_____________________。
(2)过碳酸钠(Na2CO4)中含有少量Na2O2,已知:2Na2CO4+2H2SO4![]() 2Na2SO4+2CO2↑ + O2↑ +2H2O为测定其纯度,甲、乙两位同学各称取m g该样品选用下列图示仪器药品进行实验,甲的仪器连接顺序是①⑦③⑥④ ,乙同学是①②。
2Na2SO4+2CO2↑ + O2↑ +2H2O为测定其纯度,甲、乙两位同学各称取m g该样品选用下列图示仪器药品进行实验,甲的仪器连接顺序是①⑦③⑥④ ,乙同学是①②。
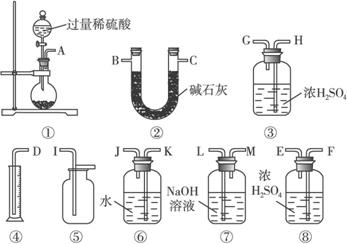
请回答下列问题:
①甲同学想通过实验测得的数据是________________,他使用装置③________________(填“有”或“没有”)必要。
②乙同学想测得的数据是________________。
③考虑到装置①中的水蒸气和空气中的水蒸气都会被装置②吸收,按乙测得的数据计算出的结果不准确,为此,请你帮助乙同学将实验装置进行改进,要求只能选用上列仪器,且每种仪器最多只能使用一次,写出各仪器接口的连接顺序________________。
④按你设计的实验装置进行实验,若所得实验前后装置②的质量分别是w
⑤由于受到仪器的限制,你帮乙改进后的装置所测得的过碳酸钠的质量分数仍稍偏低, 其原因是________________________________________________。
(1) 称取一定质量样品,向其中加入足量的盐酸,将所得溶液蒸干,称量所得固体质量,用所得固体质量、样品的质量计算样品中Na2CO3的质量,进而求得Na2CO3的质量分数
(2)①O2的体积 没有
②CO2的质量
③ AHGBCFE或 AFEBCHG(B、C可互换)
④![]() ×100%
×100%
⑤装置中的CO2不能全部被碱石灰吸收
解析:(1)先称量一定量样品,向其中加入足量稀盐酸搅拌,使之充分反应,将所得溶液蒸干,称量所得固体,然后计算出Na2CO3的质量,最后求出Na2CO3的质量分数。
(2)①测得O2的体积,无必要用③
②乙测得CO2的质量
③AHGBCFE或AFEBCHG
④Na2CO4—CO2
122 44
m(Na2CO4) w2-w1
m(Na2CO4)=![]()
w(Na2CO4)=![]() ×100%。
×100%。
⑤装置中的CO2不能全部被碱石灰吸收,仍然在仪器中有残留。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案


