题目内容
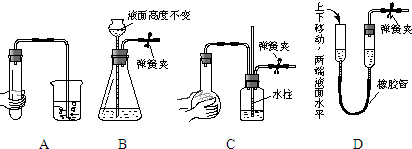
在化学实验中同一套实验装置可以用于不同的实验。下图所示装置可以完成以下实验:

A.锌片纯度的测定;
B.醇中羟基数的测定;
C.盐酸的物质的量浓度的测定;
D.NaOH溶液的物质的量浓度的测定。
现在在标准状况下进行实验。可供选择的试剂有Na、Al、Zn(含杂质)、分子式为C2H6O2的有机物、水、未知浓度的盐酸、未知浓度的NaOH溶液等。
(1)这四个实验中需要共同测定的量是
________________________________________________________________________;
(2)测定过程中,根据测定目的的不同,反应物的用量很重要,而且是实验成败的关键之一,比如实验A中盐酸要过量,实验B中________要过量,实验D中________要过量;
(3)已知在B实验中消耗m g分子式为C2H6O2的有机物,在标准状况下测得气体的体积为V mL,则该有机物中的羟基数为________,若一个该有机物分子中羟基数为2,则其结构简式为________;
(4)请写出D实验所涉及的离子方程式
________________________________________________________________________
________________________________________________________________________;
(5)装置的气密性很重要,请你说明该装置的气密性的检查方法
________________________________________________________________________
________________________________________________________________________。
(1)反应放出的氢气的体积 (2)Na Al
(3)  HOCH2CH2OH
HOCH2CH2OH
(4)2Al+6H2O+2OH-=2Al(OH)4-+3H2↑
(5)连接好实验装置,往测量管中加水至两边有液面差,静置一段时间后观察,如果液面差不再发生改变,则表示气密性良好
【解析】
试题分析:(1)由Zn与盐酸反应、Na与醇反应、Zn与盐酸反应、Al与NaOH溶液反应可实现题中的四个实验。
(2)要测定乙醇中羟基的个数,则金属钠必须过量。同样要测定氢氧化钠溶液的浓度,则金属铝是过量的。
(3)由C2H6O2 ~ H2
62 g n(H2)
m g  mol
mol
可知1 mol该醇完全反应产生的H2为 ,而2 mol醇羟基产生1 mol H2,所以1个该醇分子中—OH的数目为2×
,而2 mol醇羟基产生1 mol H2,所以1个该醇分子中—OH的数目为2× 。
。
考点:考查物质含量测定的实验设计、条件控制、气密性检验以及有关计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,难易适中,侧重对学生基础知识的巩固与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,同时也注重对学生答题能力的培养和方法指导,有利于培养学生的逻辑思维能力和发散思维能力。该类试题是一类综合性较强的试题,它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法,提升学生的学科素养。

(1)下列实验操作或对实验事实的描述不正确的有 (填序号)。
A.用托盘天平称量17.55g氯化钠晶体
B.碳酸钠溶液保存在带玻璃塞的试剂瓶
C.用干燥的pH试纸测定新制氯水的pH
D.使用容量瓶配制溶液时,俯视刻度线定容后浓度偏大
E.向饱和FeCl3溶液中滴加少量NaOH溶液,可制取Fe(OH)3胶体
F.除去CO2气体中混有的少量HCl,可以将气体通入饱和碳酸氢钠溶液
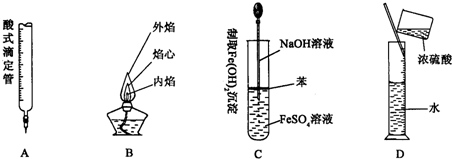
(2)下图为中学化学实验中常见的实验装置



A B C
实验室常用装置A制备下表中气体,请将分液漏斗和圆底烧瓶中应装的化学试剂填写完整。
|
气体 |
O2 |
Cl2 |
NH3 |
|
分液漏斗中试剂 |
|
|
浓氨水 |
|
圆底烧瓶中试剂 |
|
KMnO4 |
|
可用B装置排液收集气体,气体应从该装置________(填“左”“右”)管口导进,倘若利用该装置收集Cl2,试剂瓶中盛放的试剂为 。
C装置用于处理多余气体对环境的污染,若利用该装置吸收Cl2,此时烧杯中发生反应的离子方程式为 。倘若该装置中仅仅盛放稀硫酸,通常不适合吸收氨气的原因是 ,若向烧杯中额外再加入一种液态有机物则可安全吸收氨气,这种有机物为 。