题目内容
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.①用
②该实验应选用
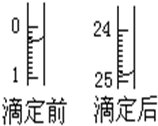
(2)如图表示第二次滴定时50mL滴定管中前后液面的位置.用去的标准盐酸消耗的体积为
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果
考点:中和滴定
专题:
分析:(1)根据酸性溶液存放在酸式滴定管中;
②根据NaOH溶液和盐酸溶液恰好反应后呈中性,可以选择酸性或碱性变色范围内的指示剂;
(2)根据滴定管的结构以及测量体积的原理来分析;
(3)根据c(待测)=
分析不当操作对c(待测)的影响,以此判断浓度的误差;
②根据NaOH溶液和盐酸溶液恰好反应后呈中性,可以选择酸性或碱性变色范围内的指示剂;
(2)根据滴定管的结构以及测量体积的原理来分析;
(3)根据c(待测)=
| V(标)×c(标) |
| V(待测) |
解答:
解:(1)①盐酸是酸性溶液,存放在酸式滴定管中;
故答案为:酸;
②NaOH溶液和盐酸溶液恰好反应后呈中性,可以选择酸性变色范围内的指示剂甲基橙或碱性变色范围内的指示剂酚酞;
故答案为:酚酞或甲基橙;
(2)滴定前读数为:0.30mL,滴定后读数为:24.90mL,消耗溶液的体积为24.60mL;
故答案为:24.60;
(3)a.若滴定前用蒸馏水冲洗锥形瓶,待测液的物质的量不变,对V(标)无影响,根据c(待测)=
分析,可知c(待测)无影响;
b.读数时,若滴定前仰视,滴定后俯视,造成V(标)无偏小,根据c(待测)=
分析,可知c(待测)偏小;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,造成V(标)无偏小,根据c(待测)=
分析,可知c(待测)偏小;
故答案为:无影响;偏小;偏小;
故答案为:酸;
②NaOH溶液和盐酸溶液恰好反应后呈中性,可以选择酸性变色范围内的指示剂甲基橙或碱性变色范围内的指示剂酚酞;
故答案为:酚酞或甲基橙;
(2)滴定前读数为:0.30mL,滴定后读数为:24.90mL,消耗溶液的体积为24.60mL;
故答案为:24.60;
(3)a.若滴定前用蒸馏水冲洗锥形瓶,待测液的物质的量不变,对V(标)无影响,根据c(待测)=
| V(标)×c(标) |
| V(待测) |
b.读数时,若滴定前仰视,滴定后俯视,造成V(标)无偏小,根据c(待测)=
| V(标)×c(标) |
| V(待测) |
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,造成V(标)无偏小,根据c(待测)=
| V(标)×c(标) |
| V(待测) |
故答案为:无影响;偏小;偏小;
点评:本题主要考查了酸碱中和滴定的操作、误差分析,难度中等,掌握中和滴定的原理是解题的关键.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
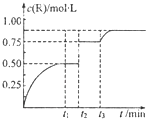 一定温度下,将1molN气体充入2L恒容密闭容器中,发生反应:M(g)+N(g)?xR(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体R的浓度随时间变化如图所示.下列说法正确的是( )
一定温度下,将1molN气体充入2L恒容密闭容器中,发生反应:M(g)+N(g)?xR(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体R的浓度随时间变化如图所示.下列说法正确的是( )| A、该反应方程式中:x=1 |
| B、t1~t3间该反应的平衡常系数均为4 |
| C、t2时刻改变的条件是使用催化剂 |
| D、t3时刻改变的条件是移去少量Q |
已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
| A、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2b kJ?mol-1 | ||
B、C2H2(g)+
| ||
| C、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-4b kJ?mol-1 | ||
| D、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+b kJ?mol-1 |
已知2Cu(NO3)2
2CuO+4NO2↑+O2↑;已知带火星的木条在空气中不能复燃,但伸进分解产生的混合气体中,木条能复燃,分析说明( )
| ||
| A、NO2具有氧化性 |
| B、NO2具有还原性 |
| C、NO2不发生反应 |
| D、只有O2才能燃烧 |
将11.2g的MgCu混合物完全溶解于足量的硝酸中,收集反应产生的X气体.再向所得溶液中加入适量的氢氧化钠溶液,产生21.4g沉淀.根据题意推断气体X的成分可能是( )
| A、0.3 mol NO2和0.3 mol NO |
| B、0.1 mol NO、0.2 mol NO2和0.05 mol N2O4 |
| C、0.2 mol NO2和0.1 mol N2O4 |
| D、0.6 mol NO |
碳原子数小于或等于8的单烯烃,与HBr加成反应的产物只有一种结构,符合条件的单烯烃(不考虑反异构和立体异构)( )
| A、4种 | B、5种 | C、6种 | D、7种 |
 ,
,