题目内容
19.有①CH3COOH;②HCl;③H2SO4 三种酸.(1)CH3COOH溶液中,其电离平衡常数表达式为K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$
(2)0.1mol/L的三种酸溶液,c(H+)由大到小的排列顺序是③>②>①(填序号).
(3)体积相同、c(H+)相同的三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是①>②=③(填序号).
(4)将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为①>②=③;
(5)已知,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.实验测得稀醋酸与稀NaOH溶液反应生成1mol H2O时放出57kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H=+0.3 kJ/mol.
分析 (1)电离平衡常数表达式为:K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$;
(2)浓度相同,溶液中氢离子浓度大小按①CH3COOH是一元弱酸,部分电离;②HCl一元强酸,完全电离;③H2SO4二元强酸,完全电离;
(3)c(H+)相同的盐酸和硫酸中和碱的能力相同,而盐酸和醋酸,因为醋酸是弱电解质,所以醋酸中和碱的能力强;
(4)醋酸是弱电解质加水稀释促进电离,所以稀释后醋酸氢离子浓度最大,而盐酸和硫酸氢离子的浓度只减小;
(5)利用盖斯定律计算反应热.
解答 解:(1)电离平衡常数表达式为:K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$,故答案为:$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$;
(2)浓度相同,溶液中氢离子浓度大小按①CH3COOH是一元弱酸,部分电离;②HCl一元强酸,完全电离;③H2SO4二元强酸,完全电离,所以氢离子浓度最大的是硫酸,最小的是醋酸,所以大到小的排列顺序是③>②>①,故答案为:③>②>①;
(3)c(H+)相同的盐酸和硫酸中和碱的能力相同,而盐酸和醋酸,因为醋酸是弱电解质,所以醋酸中和碱的能力强,所以消耗NaOH溶液的体积由大到小的排列顺序为:①>②=③,故答案为:①>②=③;
(4)醋酸是弱电解质加水稀释促进电离,所以稀释后醋酸氢离子浓度最大,而盐酸和硫酸氢离子的浓度只减小,所以c(H+)由大到小的顺序为①>②=③,故答案为:①>②=③;
(5)实验测得稀醋酸与稀NaOH溶液反应生成1mol H2O时放出57kJ的热,则热化学方程式为:CH3COOH(aq)+OH-(aq)=H2O(l)+CH3COO-(aq)△H=-57.0kJ/mol…①;而H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ/mol…②;由盖斯定律①-②得CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H=+0.3 kJ/mol,
故答案为:CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H=+0.3 kJ/mol.
点评 本题考查弱电解质的电离,题目难度不大,本题注意把握弱电解质的电离特点,根据电离平衡常数应用.

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案| A. | -44.2 kJ/mol | B. | +44.2 kJ/mol | C. | -330 kJ/mol | D. | +330 kJ/mol |
| A. | 加入适量醋酸钠晶体后,两溶液的pH均增大 | |
| B. | 将温度升高至50℃,两溶液的pH均不变 | |
| C. | 加水稀释至原体积的2倍后,两溶液的pH均减小 | |
| D. | 加入足量锌粉充分反应后,两溶液产生氢气一样多 |
 的一氯化物共有(不考虑立体异构)( )
的一氯化物共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 7种 |
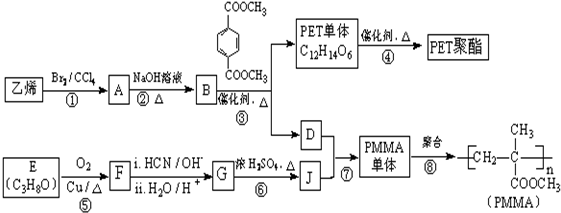
 ,它是重要的化工原料,它在一定条件下可发生以下变化:
,它是重要的化工原料,它在一定条件下可发生以下变化:
 或
或 .
. +n NH2CH2(CH2)4CH2NH2$\stackrel{一定条件}{→}$
+n NH2CH2(CH2)4CH2NH2$\stackrel{一定条件}{→}$ +(2n-1)H2O.
+(2n-1)H2O. .
.
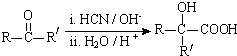 (R、R′代表烃基,可相同也可不同)
(R、R′代表烃基,可相同也可不同)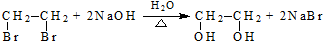 .
. .
. .
. .
. .
.
 .
.