题目内容
17.已知甲醛(HCHO)分子中的4个原子共平面的.下列分子中所有原子不可能同时存在于同一个平面上的是( )| A. |  | B. |  | C. |  | D. |  |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断,注意结合信息中甲醛的平面结构.
解答 解:A.苯为平面结构,乙烯为平面结构,通过旋转乙烯基连接苯环的单键,可以使两个平面共面,故苯乙烯中所有的原子可能处于同一平面,故A错误;
B.分子中存在甲基,具有甲烷的四面体结构,所有原子不可能处于同一平面,故B正确;
C.苯环为平面结构,醛基为平面结构,通过旋转醛基连接苯环的单键,可以使两个平面共面,故苯甲醛中所有的原子可能处于同一平面,故C错误;
D.旋转羧基中的C-O单键,可以使羧基中的所有原子处于同一平面,通过旋转羧基连接苯环的单键,可以使两个平面共面,故苯甲酸中所有的原子可能处于同一平面,故D错误.
故选B.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,其中单键可以旋转,题目难度不大.

练习册系列答案
相关题目
7.一段时间以来,各地巨能钙事件沸沸扬扬,原因在于部分巨能钙被检出含有双氧水,而双氧水有致癌性.因此卫生部已开始加紧调查巨能钙.下列有关说法错误的是( )
| A. | H2O2、Na2O2都属于过氧化物,都存在非极性的共价键 | |
| B. | 双氧水是绿色氧化剂,可作医疗消毒剂 | |
| C. | H2O2既有氧化性,又有还原性,与Cl2、KMnO4反应是表现H2O2的氧化性 | |
| D. | H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似,与SO2不同 |
8.在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol•Lˉ1、0.3mol•Lˉ1、0.2mol•Lˉ1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是(mol•Lˉ1)( )
| A. | Z为0.3 | B. | Y2为0.4 | C. | X2为0.2 | D. | Z为0.4 |
5.通过下列有关实验研究影响化学反应速率的因素得出的相关结论,你认为不正确的是( )
| A. | 在其它条件相同时,将等质量的锌块和锌粉与相同浓度的盐酸反应,锌粉反应快 | |
| B. | 将质量相同、形状大小一样的铝条分别与稀硫酸和浓硫酸反应,浓硫酸产生氢气快 | |
| C. | 两支试管中分别加入双氧水,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 | |
| D. | 在稀硫酸和铁粉反应制取氢气时,加入适量醋酸钠晶体,可减慢反应速率 |
2.“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质.Al65Cu23Fe12是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能.下列有关这种拟晶的说法正确的是( )
| A. | 无法确定Al65Cu23Fe12中三种金属的化合价 | |
| B. | Al65Cu23Fe12的硬度小于金属铁 | |
| C. | Al65Cu23Fe12不可用作长期浸泡在海水中的材料 | |
| D. | 1mol Al65Cu23Fe12溶于过量的硝酸时共失去265 mol电子 |
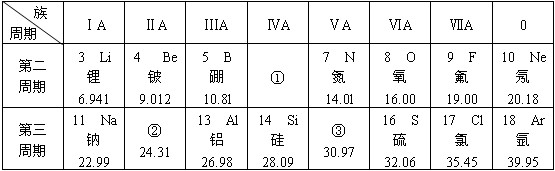
9.元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.单质的熔点降低 d.氧化物对应的水合物碱性减弱,酸性增强
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是Na+.
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是MgO的熔点高,熔融时消耗更多能量,增加生产成本;制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融态氯化铝难导电.
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式2H2(g)+SiCl4(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025akJ•mol-1.
;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式2H2(g)+SiCl4(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025akJ•mol-1.
(5)下列气体不能用浓硫酸干燥,可用P2O5干燥的是b.
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.单质的熔点降低 d.氧化物对应的水合物碱性减弱,酸性增强
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是Na+.
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
写出SiCl4的电子式:
 ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式2H2(g)+SiCl4(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025akJ•mol-1.
;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式2H2(g)+SiCl4(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025akJ•mol-1.(5)下列气体不能用浓硫酸干燥,可用P2O5干燥的是b.
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
6.按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物.下列反应符合“原子经济”原理的是( )
| A. | Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| B. | Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | |
| C. | CH2=CH2+Br2→BrCH2-CH2Br | |
| D. | 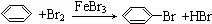 |
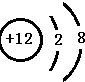 .
.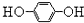 1,4一二羟基蒽醌结构简式
1,4一二羟基蒽醌结构简式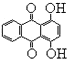
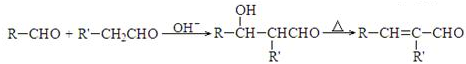
 .
. .
.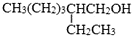 )反应可以制得另一种塑化剂DEHP.参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线.
)反应可以制得另一种塑化剂DEHP.参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线.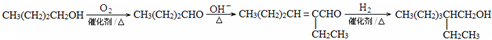 .
.