题目内容
16.设阿伏加德罗常数为NA,则下列说法正确的是( )| A. | 15g甲基(-CH3)所含有的电子数是NA | |
| B. | 常温常压下,4g氦气所含有的原子数目为NA | |
| C. | 标准状况下,1L正戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
分析 A、求出甲基的物质的量,然后根据1mol甲基中含9mol电子来分析;
B、氦气由氦原子构成;
C、标况下正戊烷为液态;
D、丙烷中含10条共价键.
解答 解:A、15g甲基的物质的量为1mol,而1mol甲基中含9mol电子,故含9NA个,故A错误;
B、氦气由氦原子构成,故4g氦气中含有的氦原子的物质的量为1mol,则为NA个,故B正确;
C、标况下正戊烷为液态,故不能根据气体摩尔体积来计算其物质的量和燃烧后的分子个数,故C错误;
D、丙烷中含10条共价键,故1mol丙烷中含10NA条共价键,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
6.碱金属具有特征的性质是( )
| A. | 具有银白色金属光泽 | B. | 良好的导热性 | ||
| C. | 较强的还原性 | D. | 优良的导电性 |
1.下列物质的电子式书写正确的是( )
| A. | Na:O:H | B. | Na+[:O:H]- | C. | N::N | D. | H+[:Cl:]- |
8. 是某原子的结构示意图,下列关于该原子的描述正确的是( )
是某原子的结构示意图,下列关于该原子的描述正确的是( )
 是某原子的结构示意图,下列关于该原子的描述正确的是( )
是某原子的结构示意图,下列关于该原子的描述正确的是( )| A. | 容易得到电子 | B. | 属于非金属原子 | ||
| C. | 核电荷数为11 | D. | 最外层电子数为11 |
5.部分短周期元素的有关信息如表所示
根据表中信息,判断以下叙述正确的是( )
| 元素代号 | 元素性质或原子结构 |
| T | 第二层上的电子数是第一层的3倍 |
| R | 与T 同一族 |
| L | L2+与T2-的核外电子数相等 |
| Z | 元素最高正价是+3价,与L同周期 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | 单质与稀盐酸反应的速率为L<Z | |
| C. | Z与T形成的化合物具有两性 | |
| D. | L与R通过离子键形成的化合物阴阳离子的核外电子数相等 |
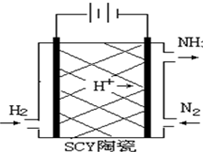 科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是反应式为N2+6H++6e-=2NH3.
科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是反应式为N2+6H++6e-=2NH3.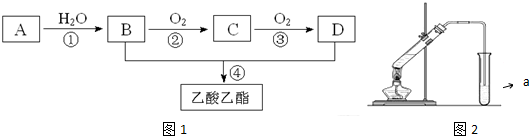
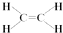 ,C的结构简式:CH3CHO.
,C的结构简式:CH3CHO.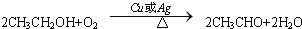 ;反应类型:氧化反应.
;反应类型:氧化反应.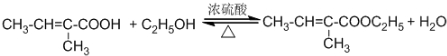 ,为从该实验后的混合气体中分离出乙酸乙酯,右侧试管中所选用的试剂a是饱和碳酸钠溶液,a试剂的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分层析出.
,为从该实验后的混合气体中分离出乙酸乙酯,右侧试管中所选用的试剂a是饱和碳酸钠溶液,a试剂的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分层析出.