题目内容
海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列.已知从海水中提取食盐和溴的过程如下:

(1)步骤Ⅱ用SO2的水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为________,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是________.
(2)某化学研究性学习小组为了从工业溴中提纯溴,查阅了有关资料:Br2的沸点是59℃,微溶于水,有毒性和强腐蚀性.他们参观了生产过程后,绘制了下图所示的装置简图.

请你参与分析讨论:
①图中仪器
B的名称是________;②整套装置的仪器连接处均不能用橡胶塞和橡胶管,原因是
________;③若装置的气密性良好,要达到提纯溴的目的,操作中应注意
________;④
C中液体的颜色是________.为除去产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后进行________(填操作名称).
答案:
解析:
 4H++SO42-+2Br- 强酸对设备的腐蚀
4H++SO42-+2Br- 强酸对设备的腐蚀
 4H++SO42-+2Br-,会产生大量的酸腐蚀设备.(2)可以联系蒸馏原理分析新情境问题.
4H++SO42-+2Br-,会产生大量的酸腐蚀设备.(2)可以联系蒸馏原理分析新情境问题.
解析:
答案:
(1)Br2+SO2+2H2O(2)①冷凝管 ②溴会腐蚀橡胶 ③控制温度计b的温度,并收集59℃时的馏分 ④深红棕色 分液(或蒸馏)
讲析:
(1)由于Br2+SO2+2H2O点评:本题以淡化海水为载体,联系化工产品的制备、环境保护等问题考查同学们对化学反应原理的认识.同时,本题将教材中介绍的分离混合物的方法——“蒸馏”、“分液”原理迁移到新情境问题中,考查大家的综合运用能力.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
海水是巨大的资源宝库,下列关于海水综合利用的说法错误的是( )
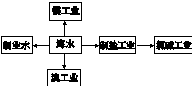

| A、海水制淡水主要有蒸馏法、电渗析法、离子交换法等 | B、海水制盐、发展氯碱工业都是发生物理变化 | C、海水提溴过程中先通入Cl2将溴离子氧化为溴单质 | D、工业上用电解熔融MgCl2的方法制取金属镁 |




