题目内容
17.(1)第三周期元素中,化学性质最不活泼的是Ar,可用于制半导体材料的元素是Si(2)Cl元素在元素周期表中的位置是第三周期VIIA.
(3)第三周期元素中元素中,最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3;
(4)在C、N、O、F中,原子半径最大的是C.
分析 (1)稀有气体原子最外层为稳定结构,化学性质最不活泼;可用于制半导体材料的元素是硅;
(2)氯元素的核电荷数为17,核外电子层数为3,最外层含有7个电子;
(3)非金属性越强,最高价氧化物对应水合物的酸性,金属性越强,最高价氧化物对应水合物的碱性越强;第三周期中铝的氢氧化物呈两性;
(4)同一周期元素,核电荷数越大,原子半径越小.
解答 解:(1)第三周期元素中,化学性质最不活泼的为稀有气体Ar;可作半导体材料的为Si,
故答案为:Ar;Si;
(2)Cl元素的核电荷数为17,在元素周期表中的位于第三周期VIIA族,
故答案为:第三周期VIIA族;
(3)第三周期元素中元素中,金属性最强的为Na,则最高价氧化物的水化物碱性最强的是NaOH;Cl的非金属性最强,则最高价氧化物对应水合物酸性最强的为:HClO4;第三周期中氢氧化铝呈两性的为Al(OH)3,
故答案为:NaOH;HClO4;Al(OH)3;
(4)C、N、O、F位于第二周期,核外电子层数相同,核电荷数越大,原子半径越小,则原子半径最大的为C,
故答案为:C.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律内容、元素周期表结构为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
7.分析如图,不能得出的结论是( )
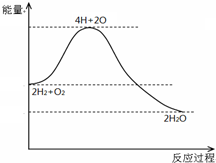

| A. | H2与O2反应是放热反应 | |
| B. | 断开化学键要放出能量 | |
| C. | 化学反应伴随着物质变化和能量变化 | |
| D. | 2mol H2和1mol O2具有的总能量高于2mol H2O 的总能量 |
8.核聚变是人类未来获取能源的理想方式之一.人类从受控热核聚变反应中可得到无穷无尽的清洁能源,相当于为自己制造了一个个小太阳.下列关于能量转换的认识中不正确的是( )
| A. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| B. | 绿色植物进行光合作用时,太阳能转化为化学能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 白炽灯工作时,电能全部转化为光能 |
5.下列说法不正确的是( )
| A. | 化学电池的反应基础是氧化还原反应 | |
| B. | 铅蓄电池是二次电池 | |
| C. | 燃料电池是一种高效,但是污染环境的发电装置 | |
| D. | 锌锰干电池是一次性电池 |
12.下列反应方程式书写正确的是( )
| A. | 甲醛和足量银氨溶液充分反应:HCHO+2Ag(NH3)2++2O- $\stackrel{加热}{→}$ HCOO-+NH4++2Ag↓+H2O+3NH3 | |
| B. | 往苯酚钠溶液中通入少量二氧化碳气体: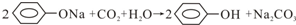 | |
| C. | 向盛有硫酸铜水溶液的试管里加入过量氨水:Cu2++4NH3•H2O═[Cu(NH3)4]2++4H2O | |
| D. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ |
2.0.6mol锌粉跟过量盐酸反应,在一定温度下,为加快反应速率但又不影响生成氢气的总量,可向反应混合物中加入适量的( )
| A. | 铜粉 | B. | 醋酸锌溶液 | C. | 氯化铜固体 | D. | 二氧化锰 |
9.2015年03月02日,全球首批3万部石墨烯手机在渝发布,石墨烯是从石墨材料中剥离出来、由碳原子组成的只有一层原子厚度的二维晶体.有关石墨烯的说法不正确的是( )
| A. | 金刚石、富勒烯、石墨烯互为碳元素的同素异形体 | |
| B. | 石墨烯中每一层内碳原子排列成平面正六边形 | |
| C. | 由于同素异形体是同种元素组成,所以石墨转化为金刚石属于物理变化 | |
| D. | 金刚石属于原子晶体,由C60构成的晶体属于分子晶体 |
6.如图是元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )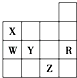

| A. | 常压下五种元素的单质中Z单质的沸点最高 | |
| B. | X元素形成的气态氢化物比W形成的气态氢化物稳定 | |
| C. | 氯离子的还原性比Y2-元素的简单阴离子的还原性强 | |
| D. | Y元素的非金属性比W元素的非金属性弱 |
7.分子式为C8H14O4的有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则符合该条件的有机物有(不考虑立体异构)( )
| A. | 16 种 | B. | 13 种 | C. | 10 | D. | 8 |