题目内容
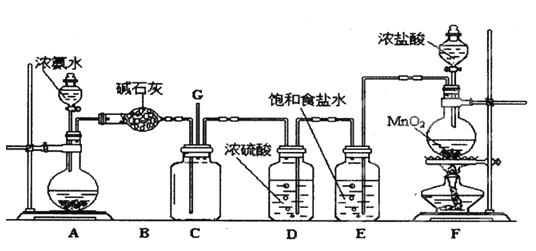
【题目】某学生利用以下装置探究氯气与氨之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。
请回答下列问题:
(1)装置F中发生反应的化学方程式为____________________________.
(2)装置B中仪器的名称是___________;装置E的作用是______________________.
(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式___________________________________.
(4)装置C内当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为_______mol-1(用含a、b的代数式表示)。
(5)将用F、E、D装置制得的氯气通人含74gCa(OH)2的石灰乳中,最多可制得漂白粉_______g.
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 干燥管 除去氯气中的氯化氢 3Cl2 + 8NH3 = N2 + 6NH4Cl b/2a 127
MnCl2+Cl2↑+2H2O 干燥管 除去氯气中的氯化氢 3Cl2 + 8NH3 = N2 + 6NH4Cl b/2a 127
【解析】
(1)二氧化锰可以和浓盐酸在加热条件下生成氯气、二氧化锰和水;
(2)根据图象可知B为干燥管,饱和食盐水可以除去氯气中的氯化氢杂质;
(3)由题意可知发生反应为氨气和氯气生成氯化铵和氮气;
(4)由反应方程式,可知Cl2→2NH4Cl,化合价降低得到2个电子,所以1molCl2得2mol电子,根据氯气求出电子的物质的量,再根据电子的个数求出NA;
(5)根据氢氧化钙的物质的量和反应方程式求出漂白粉的质量;
(1)二氧化锰可以和浓盐酸在加热条件下生成氯气、二氧化锰和水,其反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)根据图象可知B为干燥管,饱和食盐水可以除去氯气中的氯化氢杂质,故答案为:干燥管;除去氯气中的氯化氢;
(3)氨气和氯气反应生成白烟氯化铵和空气的主要成分之一氮气,即8NH3+3Cl2═6NH4Cl+N2,故答案为:8NH3+3Cl2═6NH4Cl+N2;
(4)由反应方程式可知Cl2→2NH4Cl,化合价降低得到2个电子,所以1molCl2得2mol电子,所以当有a mol氯气参加反应时,转移的电子的物质的量为2amol,已知转移的电子总数为b个,则N=nNA,即b=2aNA,所以NA=![]() ,故答案为:
,故答案为:![]() ;
;
(5)氢氧化钙的物质的量是n=![]() =1mol,所以根据反应式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知,则生成的CaCl2、Ca(ClO)2各0.5mol,所以最多可制得漂白粉的质量是m=m(CaCl2)+m(Ca(ClO)2)=0.5mol×111g/mol+0.5mol×143g/mol=127g,故答案为:127g.
=1mol,所以根据反应式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知,则生成的CaCl2、Ca(ClO)2各0.5mol,所以最多可制得漂白粉的质量是m=m(CaCl2)+m(Ca(ClO)2)=0.5mol×111g/mol+0.5mol×143g/mol=127g,故答案为:127g.