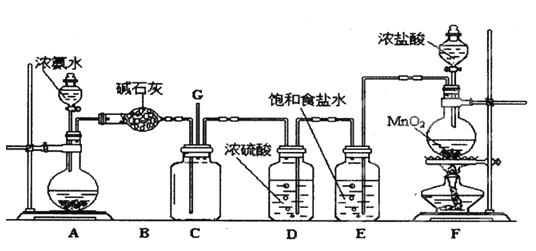
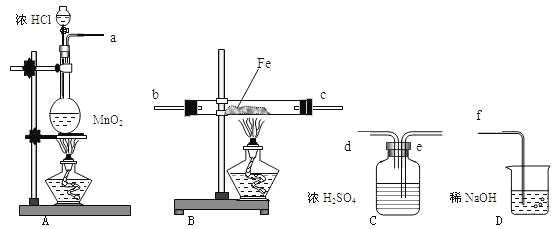
ЬтФПФкШн
ЁОЬтФПЁПИљОнЯТСаЭМЪОЫљЕУГіЕФНсТле§ШЗЕФЪЧ
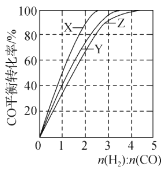
A.ЯТЭМЪЧдкВЛЭЌЮТЖШЯТШ§ИіКуШнШнЦїжаЗДгІ2H2(g)+CO(g)CH3OH(g) ЁїH<0ЕФЦНКтЧњЯпЃЌЧњЯпXЖдгІЕФЮТЖШЯрЖдНЯИп
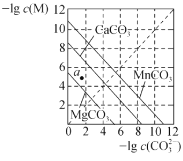
B.ЯТЭМЪЧвЛЖЈЮТЖШЯТШ§жжЬМЫсбЮMCO3ЃЈMЃКMg2+ЁЂCa2+ЁЂMn2+ЃЉЕФГСЕэШмНтЦНКтЧњЯпЃЌaЕуПЩБэЪОMgCO3ЕФЙ§БЅКЭШмвКЃЌЧвc(Mg2ЃЋ)>c(CO32-)
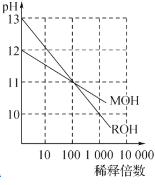
C.ЯТЭМЮЊMOHКЭROHСНжжвЛдЊМюЫЎШмвКдкГЃЮТЯТЗжБ№МгЫЎЯЁЪЭЪБpHжЕЕФБфЛЏЧњЯпЃЌПЩжЊROHЪЧЧПМю
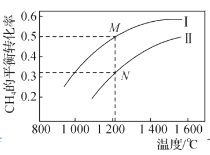
D.ЯТЭМЮЊСНИі1LШнЦїжаИїЭЖШы1molCH4КЭ1molCO2ЫљЗЂЩњЗДгІCH4(g)+CO2(g)2CO(g)+2H2(g)ЕФЦНКтЧњЯпЃЌNЕуЛЏбЇЦНКтГЃЪ§K=1
ЁОД№АИЁПC
ЁОНтЮіЁП
гІгУЦНКтвЦЖЏдРэЃЌЗжЮіЭтвђЖдЛЏбЇЦНКтЁЂГСЕэШмНтЦНКтЁЂЕчРыЦНКтЕФгАЯьЃЌХаЖЯгЩЭМЯѓЕУГіЕФНсТлЪЧЗёе§ШЗЁЃ
AЃЎдкЭМжазївЛДЙЯпЃЌгыШ§ЧњЯпИїгавЛНЛЕуЃЌБэУїдкЗДгІЮяБШР§ЯрЭЌЪБЃЌXЧњЯпЖдгІЮТЖШЯТCOЦНКтзЊЛЏТЪНЯИпЃЌЩ§ИпЮТЖШЃЌЦНКтЯђЮќШШЗНЯђвЦЖЏЃЌИУе§ЗДгІЕФІЄH<0ЮЊЗХШШЗДгІЃЌЮТЖШдНИпЃЌCOзЊЛЏТЪдНЕЭЃЌЙЪXЧњЯпЖдгІЮТЖШНЯЕЭЃЌAЯюДэЮѓЃЛ
BЃЎЙ§aЕузїДЙЯпЃЌгыMgCO3жБЯпгаНЛЕуЃЈБЅКЭШмвКЃЉЁЃПЩМћЃЌдкc(CO32-)ЯрЭЌЪБЃЌaЕуШмвКжаc(Mg2+)БШБЅКЭШмвКжаЕФаЁЃЌЮЊВЛБЅКЭШмвКЁЃaЕуЪБ-lgc(Mg2ЃЋ)>-lgc(CO32-)ЃЌдђc(Mg2ЃЋ)<c(CO32-)ЃЌBЯюДэЮѓЃЛ
CЃЎЧПМюЯЁЪЭ10nБЖЃЌpHМѕаЁnЃЌгЩЭМПЩжЊЃЌROHШмвКПЊЪМpH=13ЃЌМгЫЎЯЁЪЭ10БЖЁЂ100БЖЁЂ1000БЖЪБЃЌШмвКpHЗжБ№БфЮЊ12ЁЂ11ЁЂ10ЃЌpHЗжБ№МѕаЁ1ЁЂ2ЁЂ3ЃЌдђROHЪЧЧПМюЃЌCЯюе§ШЗЃЛ
DЃЎЛЏбЇЦНКтГЃЪ§жЛгыЮТЖШгаЙиЃЌNЕуЕФЦНКтГЃЪ§ПЩгУMЕуМЦЫуЁЃгЩЭМПЩжЊЦНКтЪБМзЭщЕФзЊЛЏТЪЮЊ0.5ЃЌгЩCH4(g)+CO2(g)2CO(g)+2H2(g)ПЩжЊЦНКтЪБCH4(g)ЁЂCO2(g)ЕФХЈЖШЖМЪЧ0.5mol/LЃЌCO(g)ЁЂH2(g)ЕФХЈЖШЖМЪЧ1mol/LЃЌдђKЃН![]() =4ЃЌDЯюДэЮѓЁЃ
=4ЃЌDЯюДэЮѓЁЃ
Д№АИбЁCЁЃ

 гХЕШЩњЬтПтЯЕСаД№АИ
гХЕШЩњЬтПтЯЕСаД№АИЁОЬтФПЁПдкЮТЖШT1КЭT2ЪБЃЌЗжБ№НЋ0.5molCH4КЭ1.2molNO2ГфШыЬхЛ§ЮЊ1LЕФУмБеШнЦїжаЃЌЗЂЩњЗДгІЃК CH4(g)ЃЋ2NO2(g)![]() N2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЃЌВтЕУгаЙиЪ§ОнШчБэЃК
N2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЃЌВтЕУгаЙиЪ§ОнШчБэЃК
ЪБМф/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | ЁЁ | 0.15 |
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.T1ЪБ0~10minNO2ЕФЦНОљЗДгІЫйТЪЮЊ0.15molЁЄLЃ1ЁЄminЃ1
B.T2ЪБCH4ЕФЦНКтзЊЛЏТЪЮЊ70.0%
C.БЃГжЦфЫћЬѕМўВЛБфЃЌT1ЪБЯђЦНКтЬхЯЕжадйГфШы0.3molCH4КЭ0.80molH2O(g)ЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ
D.БЃГжЦфЫћЬѕМўВЛБфЃЌT1ЪБЯђЦНКтЬхЯЕжадйГфШы0.5molCH4КЭ1.2molNO2ЃЌгыдЦНКтЯрБШЃЌДяаТЦНКтЪБN2ЕФХЈЖШдіДѓ