题目内容
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )

A.0.15 mol CuO B.0.1 mol CuCO3
C.0.075mol Cu(OH)2 D.0.05 mol Cu2(OH)2CO3
D
【解析】
试题分析:用惰性电极电解硫酸铜溶液,反应方程式是:2CuSO4+2H2O  2H2SO4+2Cu+O2↑,当电子转移0.2mol时CuSO4反应完全,产生0.1mol的H2SO4和0.1mol的Cu、0.05mol O2↑,再继续电解,实质就是电解水,方程式是2H2O
2H2SO4+2Cu+O2↑,当电子转移0.2mol时CuSO4反应完全,产生0.1mol的H2SO4和0.1mol的Cu、0.05mol O2↑,再继续电解,实质就是电解水,方程式是2H2O  2H2↑+O2↑,当再转移0.1mol的电子时,又消耗0.05mol的水。所以欲使溶液恢复到起始状态,根据元素守恒,进入溶液中的各种元素应该是:加入0.1mol的Cu,H:0.1mol;O: 0.05mol×3=0.15mol.当加入 0.05 mol Cu2(OH)2CO3时会产生CO2气体逸出,故增加的元素及质量符合题意,只有选项D符合题意,因此选项是D。
2H2↑+O2↑,当再转移0.1mol的电子时,又消耗0.05mol的水。所以欲使溶液恢复到起始状态,根据元素守恒,进入溶液中的各种元素应该是:加入0.1mol的Cu,H:0.1mol;O: 0.05mol×3=0.15mol.当加入 0.05 mol Cu2(OH)2CO3时会产生CO2气体逸出,故增加的元素及质量符合题意,只有选项D符合题意,因此选项是D。
考点:考查电解原理的应用的知识。

练习册系列答案
相关题目
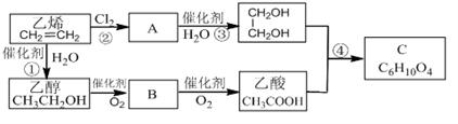
 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题: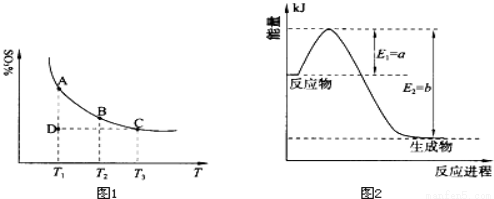
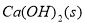
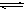
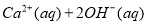 ,下列说法正确的是( )
,下列说法正确的是( )