��Ŀ����
��10�֣����û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮
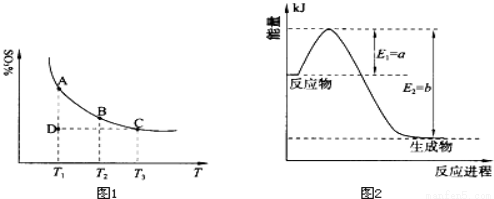
��1�����������У�SO2����������SO3��2SO2��g��+O2��g�� 2SO3��g���������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
2SO3��g���������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
�ٺ��¡���ѹ�����£���Ӧ2SO2��g��+O2��g�� 2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����ƽ�� �ƶ�������������ҡ���������
2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����ƽ�� �ƶ�������������ҡ���������
�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1 K2�����������������=������ͬ��������Ӧ���е�״̬Dʱ��v�� v�棨���������������=������
��2�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã�
����ͼ2��һ�����¶Ⱥ�ѹǿ����N2��H2��Ӧ����1molNH3�����������仯ʾ��ͼ����д����ҵ�ϳɰ����Ȼ�ѧ��Ӧ����ʽ�� ������H����ֵ�ú���ĸa��b�Ĵ���ʽ��ʾ��
�ڰ�������ˮ�õ���ˮ����25���£���a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һǡ�������ԣ��ú�a��b�Ĵ���ʽ��ʾ����ˮ�ĵ���ƽ�ⳣ������ʽ ��
��3����֪25��CʱKsp[AgCl]=1.6��10-10mol2?L-2��Ksp[AgI]=1.5��10-16mol2?L-2������25���£���0.1L0.002mol?L-1��NaCl��Һ����μ���0.1L0.002mol?L-1��������Һ���а�ɫ�������ɣ��ӳ����ܽ�ƽ��ĽǶȽ��Ͳ���������ԭ���� ����Ӧ�����Һ�У���������0.1L0.002mol?L-1��NaI��Һ�������������� �������������ԭ���ǣ������ӷ���ʽ��ʾ�� ��
��1���� ���� �� �� �� ��
��2����N2��g��+3H2��g�� 2NH3��g����H=-2��b-a��kJ?mol-1 ���� 10-7b/(a-b)��
2NH3��g����H=-2��b-a��kJ?mol-1 ���� 10-7b/(a-b)��
��3��c(Ag+)(Cl-)�����ܶȻ�Ksp��AgCl���� ��ɫ����ת��Ϊ��ɫ���� AgCl��s��+I-�TAgI��s��+Cl-��
��������
����������ٺ��¡���ѹ�����£���Ӧ2SO2��g��+O2��g�� 2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����Ϊ�˱���ѹǿ���䣬���������ݻ���Ҫ����ʹ��Ӧ��ϵ�ĸ������ʵ�Ũ�ȶ���С�����ڷ�Ӧ��ϵ����С�ı����࣬����ƽ�������ƶ�������ͼ���֪�������¶ȣ�SO3��ƽ�⺬����С��˵�������¶�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴Ӧ���������ȷ�Ӧ����˸÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ԡ�H<0����Ϊ�����¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С�����������¶�ΪT1<T2����Ӧ�ﵽƽ��״̬״̬ʱ��ƽ�ⳣ���ֱ�ΪK1>K2������Ӧ���е�״̬Dʱ����Ӧδ�ﵽ���¶��µ�ƽ��״̬��SO3�ĺ�������ƽ��״̬�����Է�Ӧ������У����v��>v��; (2)�ٸ���ͼʾ��֪�ڹ�ҵ�ϳɰ����Ȼ�ѧ��Ӧ����ʽ��N2��g��+3H2��g��
2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����Ϊ�˱���ѹǿ���䣬���������ݻ���Ҫ����ʹ��Ӧ��ϵ�ĸ������ʵ�Ũ�ȶ���С�����ڷ�Ӧ��ϵ����С�ı����࣬����ƽ�������ƶ�������ͼ���֪�������¶ȣ�SO3��ƽ�⺬����С��˵�������¶�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴Ӧ���������ȷ�Ӧ����˸÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ԡ�H<0����Ϊ�����¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С�����������¶�ΪT1<T2����Ӧ�ﵽƽ��״̬״̬ʱ��ƽ�ⳣ���ֱ�ΪK1>K2������Ӧ���е�״̬Dʱ����Ӧδ�ﵽ���¶��µ�ƽ��״̬��SO3�ĺ�������ƽ��״̬�����Է�Ӧ������У����v��>v��; (2)�ٸ���ͼʾ��֪�ڹ�ҵ�ϳɰ����Ȼ�ѧ��Ӧ����ʽ��N2��g��+3H2��g�� 2NH3��g����H=-2��b-a��kJ/mol������25���£���a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һǡ�������ԣ���c(NH4+)=c(Cl-);�������ǰ�ˮ���Ȼ�淋Ļ����Һ��NH3.H2O
2NH3��g����H=-2��b-a��kJ/mol������25���£���a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һǡ�������ԣ���c(NH4+)=c(Cl-);�������ǰ�ˮ���Ȼ�淋Ļ����Һ��NH3.H2O NH4++OH-��c(NH4+)=b/2mol/L; c(OH-)=10-7mol/L������NԪ���غ�ɵ�c(NH3.H2O)=(a��b)/2mol/L,���ð�ˮ�ĵ���ƽ�ⳣ������ʽK=
NH4++OH-��c(NH4+)=b/2mol/L; c(OH-)=10-7mol/L������NԪ���غ�ɵ�c(NH3.H2O)=(a��b)/2mol/L,���ð�ˮ�ĵ���ƽ�ⳣ������ʽK=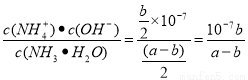 ����3����֪25��CʱKsp[AgCl]=1.6��10-10mol2?L-2��Ksp[AgI]=1.5��10-16mol2?L-2������25���£���0.1L0.002mol?L-1��NaCl��Һ����μ���0.1L0.002mol?L-1��������Һ������c(Ag+)��c(Cl-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.6��10-10mol2?L-2 =Ksp[AgCl]�������а�ɫ�������ɣ��ڸ�����Һ�д���AgCl�ij����ܽ�ƽ�⣬����Ӧ�����Һ�У���������0.1L0.002mol?L-1��NaI��Һ������c(Ag+) ��c(I-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.5��10-16 mol2?L-2 =Ksp[AgI]�����Ի����������ת������ɫ����ת��Ϊ��ɫ���������ӷ���ʽ��AgCl��s��+I-�TAgI��s��+Cl-��
����3����֪25��CʱKsp[AgCl]=1.6��10-10mol2?L-2��Ksp[AgI]=1.5��10-16mol2?L-2������25���£���0.1L0.002mol?L-1��NaCl��Һ����μ���0.1L0.002mol?L-1��������Һ������c(Ag+)��c(Cl-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.6��10-10mol2?L-2 =Ksp[AgCl]�������а�ɫ�������ɣ��ڸ�����Һ�д���AgCl�ij����ܽ�ƽ�⣬����Ӧ�����Һ�У���������0.1L0.002mol?L-1��NaI��Һ������c(Ag+) ��c(I-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.5��10-16 mol2?L-2 =Ksp[AgI]�����Ի����������ת������ɫ����ת��Ϊ��ɫ���������ӷ���ʽ��AgCl��s��+I-�TAgI��s��+Cl-��
���㣺������������Ի�ѧƽ���ƶ���Ӱ�졢�ε�ˮ�⡢������ʵ���ƽ�ⳣ���ı�������ܽ�ƽ�������Ӧ�ü�������ת����֪ʶ��

 CaO��CO2��
CaO��CO2��