题目内容
3.设NA是阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下,48gO3含有的氧原子数为NA | |
| B. | 11.2LSO3中含有的SO3分子数为NA | |
| C. | 1.8g的NH4+离子中含有的电子数为NA | |
| D. | 0.1L2mol/LNaCl溶液中含有Na+个数为NA |
分析 A、臭氧由氧原子构成;
B、三氧化硫所处的状态不明确;
C、求出铵根离子的物质的量,然后根据铵根离子中含10个电子来分析;
D、求出氯化钠的物质的量,然后根据氯化钠中含1个钠离子来分析.
解答 解:A、臭氧由氧原子构成,故48g臭氧中含有的氧原子的物质的量为3mol,故含3NA个,故A错误;
B、三氧化硫所处的状态不明确,不一定是气体,故其物质的量无法计算,故B错误;
C、1.8g铵根离子的物质的量为0.1mol,而铵根离子中含10个电子,故0.1mol铵根离子中含NA个电子,故C正确;
D、溶液中氯化钠的物质的量n=CV=2mol/L×0.1L=0.2mol,而氯化钠中含1个钠离子,故0.2mol氯化钠中含0.2NA个钠离子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
13.分枝酸可用于生化研究.其结构简式如图,下列关于分枝酸的叙述正确的是( )
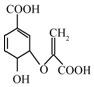

| A. | 分子式为C9H10O6 | |
| B. | 可与乙醇、乙酸反应,且反应类型相同 | |
| C. | 可使溴的四氧化碳溶液,酸性高锰酸钾溶液褪色,且原理相同 | |
| D. | 分子中含有三种官能团 |
14.下列离子方程式书写正确的是( )
| A. | 氯化铝溶液与过量氨水的反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 氯水与碘化钾溶液的反应:Cl2+2I-═2Cl-+I2 | |
| C. | 铁粉与足量稀硫酸的反应:2Fe+3H+═2Fe3++3H2↑ | |
| D. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
11.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol•L-1的NaOH溶液:K+、Ba2+、Cl-、NO3- | |
| B. | 0.1mol•L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1mol•L-1的FeCl3溶液:K+、NH4+、NO3-、Cl- | |
| D. | 0.1mol•L-1的HCl溶液:K+、Na2+、SO42-、CO32- |
18.单晶硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质).粗硅与氯气反应生成四氯化硅(反应温度450:500℃)四氯化硅经提纯后用氢气还原可得高纯硅.以下是实验室制备四氯化硅的装置示意图.
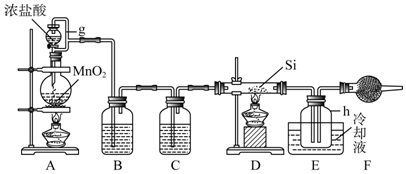
相关信息如下:
a.四氯化硅遇水极易反应;
b.硝、铝、铁、磷在高温下均能与氧气直接反应生成相应的氯化物;
c.有关物质的物理常数见表:
请回答下列问题:
(1)写出装置A中反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;制备粗硅的化学反应方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(2)装置B中的试剂是饱和食盐水;装置C中的试剂是浓硫酸;装置E中的h瓶需要冷却理由是产物SiCl4沸点低,需要冷凝收集;干燥管F中碱石灰的作用是吸收空气中的水蒸气.
(3)装置E中h瓶收集到的粗产物含有多种杂质:BCl3、AlCl3、FeCl3、PCl3,根据题给信息,可通过蒸馏(填操作名称),得到高纯度四氯化硅.
(4)从二氧化硅到高纯硅的生产流程中,经历了一系列氧化还原反.涉及多种含硅物质,这些含硅的物质中,作为氧化剂的有SiO2、SiCl4;作为还原剂的有Si.

相关信息如下:
a.四氯化硅遇水极易反应;
b.硝、铝、铁、磷在高温下均能与氧气直接反应生成相应的氯化物;
c.有关物质的物理常数见表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl3 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -17.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 163 |
(1)写出装置A中反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;制备粗硅的化学反应方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(2)装置B中的试剂是饱和食盐水;装置C中的试剂是浓硫酸;装置E中的h瓶需要冷却理由是产物SiCl4沸点低,需要冷凝收集;干燥管F中碱石灰的作用是吸收空气中的水蒸气.
(3)装置E中h瓶收集到的粗产物含有多种杂质:BCl3、AlCl3、FeCl3、PCl3,根据题给信息,可通过蒸馏(填操作名称),得到高纯度四氯化硅.
(4)从二氧化硅到高纯硅的生产流程中,经历了一系列氧化还原反.涉及多种含硅物质,这些含硅的物质中,作为氧化剂的有SiO2、SiCl4;作为还原剂的有Si.
8.下列有关物质的性质或用途的说法中,不正确的是( )
①氯水具有漂白性,可以是湿润有色布条褪色
②可溶性铁盐铝盐可用于净水
③Si-可用与制造光导纤维
④SiO2、Na2CO3和CaCO3可用于制玻璃
⑤水玻璃可用与生产防火材料
⑥铁红常用作红色油漆和涂料.
①氯水具有漂白性,可以是湿润有色布条褪色
②可溶性铁盐铝盐可用于净水
③Si-可用与制造光导纤维
④SiO2、Na2CO3和CaCO3可用于制玻璃
⑤水玻璃可用与生产防火材料
⑥铁红常用作红色油漆和涂料.
| A. | ③⑤ | B. | ④⑤ | C. | ③ | D. | ③④ |
15.(1)常温常压下,依据事实,写出下列反应的热化学方程式.
①在25℃、101kPa下,2g甲醇燃烧生成CO2和液态水时放热45kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-720kJ/mol.
②若适量的N2和O2完全反应,每生成23g NO2需要吸收17kJ热量N2(g)+2O2(g)═2NO2(g)△H=+68kJ/mol.
(2)断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ•mol-1)表是一些键能数据(KJ•mol-1)
①根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H
②根据键能和反应热化学方程式$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(g )△H=-46kJ•mol-1 计算N≡N的键能.
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(25℃、101kPa下测得的热量).
①该反应的热化学方程式为N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.75kJ/mol.
②又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是408.875 kJ.
①在25℃、101kPa下,2g甲醇燃烧生成CO2和液态水时放热45kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-720kJ/mol.
②若适量的N2和O2完全反应,每生成23g NO2需要吸收17kJ热量N2(g)+2O2(g)═2NO2(g)△H=+68kJ/mol.
(2)断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ•mol-1)表是一些键能数据(KJ•mol-1)
| 化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
| C-H | 414 | C-F | 489 | H-F | 565 | F-F | 158 |
| H-H | 436 | H-N | 391 |
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H
②根据键能和反应热化学方程式$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(g )△H=-46kJ•mol-1 计算N≡N的键能.
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(25℃、101kPa下测得的热量).
①该反应的热化学方程式为N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.75kJ/mol.
②又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是408.875 kJ.
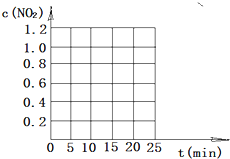 烟气的主要污染物是SO2、NOx,经臭氧预处理后再用适当溶液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
烟气的主要污染物是SO2、NOx,经臭氧预处理后再用适当溶液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为: