��Ŀ����
(11��) ��Դ��ȱ���������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ������������ַ�Ӧ�ϳɼ״���
��ӦI��CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  ��H1
��H1
��ӦII��CO(g)+2H2(g) CH3OH(g) ��H2
CH3OH(g) ��H2
��1��������Ӧ���ϡ�ԭ�Ӿ��á�ԭ����� ���������ӦI�Ļ�ѧƽ�ⳣ������ʽK= ��
��
��2���±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧ ƽ�ⳣ��(K)
ƽ�ⳣ��(K)
���ɱ��������жϦ�H2 0�����������������������
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� ��
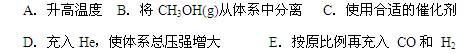
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c(CO)="0.2" mol��L-1����CO��ת����Ϊ ����ʱ���¶�Ϊ �����ϱ���ѡ��
��ӦI��CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  ��H1
��H1��ӦII��CO(g)+2H2(g)
 CH3OH(g) ��H2
CH3OH(g) ��H2��1��������Ӧ���ϡ�ԭ�Ӿ��á�ԭ����� ���������ӦI�Ļ�ѧƽ�ⳣ������ʽK=
 ��
����2���±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧ
 ƽ�ⳣ��(K)
ƽ�ⳣ��(K) | �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� ��
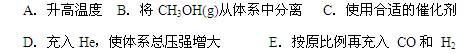
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c(CO)="0.2" mol��L-1����CO��ת����Ϊ ����ʱ���¶�Ϊ �����ϱ���ѡ��

��

��ϰ��ϵ�д�
�����Ŀ
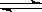 CO2��g����H2(g) ��K��1.0������Ӧ��ʼʱCO��H2O��Ũ�ȷֱ�Ϊ0.20mol/L��1.00mol/L����COת��ΪCO2��ת����Ϊ
CO2��g����H2(g) ��K��1.0������Ӧ��ʼʱCO��H2O��Ũ�ȷֱ�Ϊ0.20mol/L��1.00mol/L����COת��ΪCO2��ת����Ϊ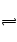 10Ca2+(aq)+6PO43-(aq)+2OH-(aq)����֪25��ʱKsp[Ca10(PO4)6(OH)2]="2.35" ��10-59�� Ksp[Ca10(PO4)6F2]=7.1�� 10-61��Ksp[CaCO3]="5" ��10-9��Ksp[CaF2]=4��10-11������˵������ȷ�ǣ� ��
10Ca2+(aq)+6PO43-(aq)+2OH-(aq)����֪25��ʱKsp[Ca10(PO4)6(OH)2]="2.35" ��10-59�� Ksp[Ca10(PO4)6F2]=7.1�� 10-61��Ksp[CaCO3]="5" ��10-9��Ksp[CaF2]=4��10-11������˵������ȷ�ǣ� ��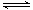 HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz��
HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz�� 3C(g)������Ӧ��ʼʱ����2 mol A��2 mol B����ƽ���A���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���A�������������a%����( )
3C(g)������Ӧ��ʼʱ����2 mol A��2 mol B����ƽ���A���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���A�������������a%����( ) 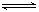 SO3(g)+NO(g���Ŀ��淴Ӧ��������˵����Ӧ�ﵽƽ��״̬���ǣ� ��
SO3(g)+NO(g���Ŀ��淴Ӧ��������˵����Ӧ�ﵽƽ��״̬���ǣ� �� Fe3O4(s)��4H2(g)����Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽΪ(����)
Fe3O4(s)��4H2(g)����Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽΪ(����) 2NH3��g��
2NH3��g��