题目内容
下列化学用语表示的几种微粒中能影响水的电离平衡,且能使水的电离平衡向右移动的是
| A.HSO4- | B.Cl- | C.aX+ | D.bX2- |
D
试题分析:水是弱电解质,存在电离平衡H2O
 H++OH-,酸或碱抑制水的电离,能水解的盐促进水的电离。A、HSO4-能完全电离出氢离子,抑制水的电离,A不正确;B、氯离子不能水解,不能促进水的电离,也不能抑制水的电离,B不正确;C、该微粒的质子数=18+1=19,即为K+,不能促进水的电离,也不能抑制水的电离,C不正确;D、该微粒的质子数=18-2=16,即为S2-。S2-水解促进水的电离,D正确,答案选D。
H++OH-,酸或碱抑制水的电离,能水解的盐促进水的电离。A、HSO4-能完全电离出氢离子,抑制水的电离,A不正确;B、氯离子不能水解,不能促进水的电离,也不能抑制水的电离,B不正确;C、该微粒的质子数=18+1=19,即为K+,不能促进水的电离,也不能抑制水的电离,C不正确;D、该微粒的质子数=18-2=16,即为S2-。S2-水解促进水的电离,D正确,答案选D。
练习册系列答案
相关题目
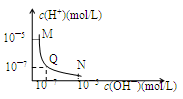
 NH3·H2O(aq)十H+(aq) ΔH=bkJ·mol-1
NH3·H2O(aq)十H+(aq) ΔH=bkJ·mol-1 =10-8,下列叙述正确的是
=10-8,下列叙述正确的是