题目内容
有下列几种物质:①Ne、②NH4Cl、③NaOH、④Cl2、⑤CO2、⑥H2O、⑦Na2O2.
(1)上述物质中,属于共价化合物的是
(2)②号物质的电子式为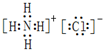
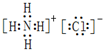 、④号物质的电子式为
、④号物质的电子式为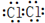
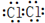 .用电子式表示⑥号物质的形成过程:
.用电子式表示⑥号物质的形成过程:
 .
.
(1)上述物质中,属于共价化合物的是
⑤⑥
⑤⑥
(填序号,下同),既存在离子键又存在极性键的是②③⑦
②③⑦
(2)②号物质的电子式为
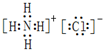
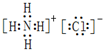
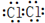
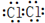


分析:(1)一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键.含有离子键的化合物就是离子化合物,全部由共价键形成的化合物是共价化合物.
(2)根据电子式的书写方法和用电子式表示物质的形成过程来完成;
(2)根据电子式的书写方法和用电子式表示物质的形成过程来完成;
解答:解:(1)因一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键.所以:②、③、⑤、⑥
中含有极性键,②、③中含有离子键和极性键,④中含有非极性键,⑦中含有离子键和非极性键,①中无化学键,含有离子键的化合物就是离子化合物,全部由共价键形成的化合物是共价化合物.所以⑤⑥是共价化合物,②③⑦是离子化合物.
故答案为:⑤⑥,②③⑦
(2)NH4Cl是离子化合物,由铵根离子和氯离子构成,其电子式为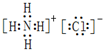 ;Cl2是共价单质,由2个氯原子构成,其电子式为
;Cl2是共价单质,由2个氯原子构成,其电子式为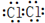 ;H2O是由2个H原子和1个O原子通过形成共用电子对形成的,形成过程为:
;H2O是由2个H原子和1个O原子通过形成共用电子对形成的,形成过程为:
故答案为: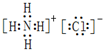 ;
;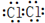 ;
;
中含有极性键,②、③中含有离子键和极性键,④中含有非极性键,⑦中含有离子键和非极性键,①中无化学键,含有离子键的化合物就是离子化合物,全部由共价键形成的化合物是共价化合物.所以⑤⑥是共价化合物,②③⑦是离子化合物.
故答案为:⑤⑥,②③⑦
(2)NH4Cl是离子化合物,由铵根离子和氯离子构成,其电子式为
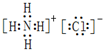 ;Cl2是共价单质,由2个氯原子构成,其电子式为
;Cl2是共价单质,由2个氯原子构成,其电子式为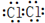 ;H2O是由2个H原子和1个O原子通过形成共用电子对形成的,形成过程为:
;H2O是由2个H原子和1个O原子通过形成共用电子对形成的,形成过程为:
故答案为:
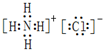 ;
;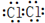 ;
;
点评:本题主要考查了化学键的判断、化学键和化合物的关系以及常用化学用语的书写.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
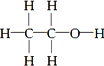
经测定,乙醇的分子式是C2H6O。由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。
① ②
②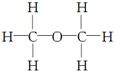
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四位同学直接利用下图给定装置进行实验确定乙醇的结构。
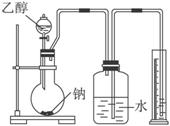
(1)学生甲得到一组实验数据,见下表:
乙醇的物质的量/mol | 氢气的体积/L |
0.10 | 1.12(标准状况) |
根据以上数据推断乙醇的结构应为______________(用①②表示),理由为______________。
(2)同学乙分别准确称量
(3)同学丙认为实验成功的关键有下列几点,其中正确的是_______________。(填序号)
①装置气密性要良好 ②实验开始前准确确定乙醇的量 ③钠足量 ④广口瓶内水必须充满 ⑤氢气体积的测算方法正确、数据准确
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么他还需知道的数据是____________。
(5)实验结束后,四名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论。如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是_______________。