题目内容
18.NaH是-种离子化合物,它跟水反应的方程式为:NaH+H2O→NaOH+H2↑,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气.下列有关NaH的叙述错误的是( )| A. | 跟水反应时,水作氧化剂 | B. | NaH在水中显酸性 | ||
| C. | 跟液氨反应时,有NaNH2生成 | D. | 跟乙醇反应时,NaH被氧化 |
分析 A.NaH+H2O═NaOH+H2↑中,NaH中的H元素由-1价升高为0,水中的H元素由+1价降低为0;
B.NaH+H2O═NaOH+H2↑生成氢氧化钠显碱性;
C.根据方程式NaH+NH3═NaNH2+H2↑判断;
D.根据方程式NaH+CH3CH2OH═CH3CH2ONa+H2↑结合NaH中的H元素由-1价升高为0判断.
解答 解:A.跟水反应时,水中H元素的化合价降低,水作氧化剂,故A正确;
B.NaH+H2O═NaOH+H2↑,所以NaH跟水反应时,生成氢氧化钠显碱性,故B错误;
C.氢化钠和液氨反应方程式为NaH+NH3═NaNH2+H2↑,故C正确;
D.跟乙醇反应时,方程式NaH+CH3CH2OH═CH3CH2ONa+H2↑,NaH中的H元素由-1价升高为0,被氧化,故D正确.
故选B.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化及氧化还原反应中的概念即可解答,题目难度不大.

练习册系列答案
相关题目
9.下列有机物命名正确的是( )
| A. |  2-甲基氯丙烷 2-甲基氯丙烷 | B. |  1,2,4-三甲苯 1,2,4-三甲苯 | C. |  2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
3.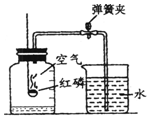 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )| A. | 该实验证明空气中氧气的质量分数约占$\frac{1}{5}$ | |
| B. | 实验时红磷要足量 | |
| C. | 实验前一定要检查装置的气密性 | |
| D. | 红磷燃烧的火焰熄灭后立刻打开弹簧夹 |
13.王老师在某次实验中制得下列四种不同质量的气体.则在他制得的四种气体中分子数目最多的是( )
| A. | 1gH2 | B. | 11gCO2 | C. | 8gO2 | D. | 4.5gH2O(g) |
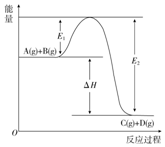 反应A(g)+B(g)═C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)═C(g)+D(g)过程中的能量变化如图所示,回答下列问题.