题目内容
已知2SO2(g)+O2(g)?2SO3(g);△H=-197KJ/mol,如果反应在密闭容器中进行,下述有关说法中正确的是( )
| A、达到平衡时,SO2的浓度与SO3的浓度相等 |
| B、相同状况下,反应2SO3(g)?2SO2(g)+O2(g)是一个吸热反应 |
| C、在密闭容器中加入2molSO2和1molO2充分反应后放出197KJ的热量 |
| D、升高温度,吸热反应的速率增大,放热反应的速率减少 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、平衡时物质的浓度与加入的多少有关;
B、2SO2(g)+O2(g)?2SO3(g);△H=-197KJ/mol,其逆反应吸热;
C、二氧化硫的催化氧化是可逆反应;
D、升温时,反应速率增大.
B、2SO2(g)+O2(g)?2SO3(g);△H=-197KJ/mol,其逆反应吸热;
C、二氧化硫的催化氧化是可逆反应;
D、升温时,反应速率增大.
解答:
解:A、平衡时SO2的浓度与SO3的浓度有加入的多少决定,不一定相等,故A错误;
B、2SO2(g)+O2(g)?2SO3(g);△H=-197KJ/mol,其逆反应吸热,故B正确;
C、二氧化硫的催化氧化是可逆反应,2molSO2和1molO2充分反应后放出的热量小于197KJ,故C错误;
D、升温时,正逆反应速率都增大,故D错误,
故选B.
B、2SO2(g)+O2(g)?2SO3(g);△H=-197KJ/mol,其逆反应吸热,故B正确;
C、二氧化硫的催化氧化是可逆反应,2molSO2和1molO2充分反应后放出的热量小于197KJ,故C错误;
D、升温时,正逆反应速率都增大,故D错误,
故选B.
点评:本题考查影响化学平衡的因素,注意温度、浓度对反应速率及平衡的影响,选项C为解答的难度,题目难度中等.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
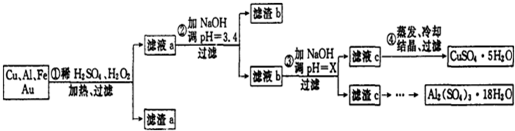
常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、NO2-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如图所示:
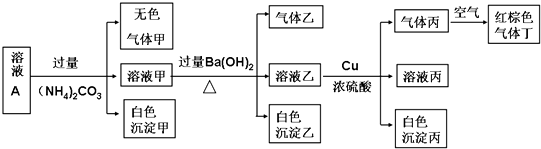
下列有关说法正确的是( )

下列有关说法正确的是( )
| A、沉淀乙一定有BaCO3,可能有BaSO4 |
| B、实验消耗Cu 14.4g,则生成气体丁的体积为3.36L |
| C、该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子 |
| D、生成的甲、乙、丙气体均为无色的易溶于水气体 |
某工业废水含有下列离子中的5种(不考虑水的电离及离子的水解),K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且各种离子的物质的量浓度相等.甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察有紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察有紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
| A、溶液中难以确定Cl-的存在与否 |
| B、原溶液中所含的离子为:Fe2+、K+、NO3-、SO42- |
| C、步骤②中可以确定Fe2+、NO3-的存在,不能确定其它离子是否存在 |
| D、步骤③中的白色沉淀为2种钡盐 |
下列化合物在自然界能稳定存在的是( )
| A、Na2O |
| B、Na2O2 |
| C、NaClO |
| D、NaCl |
下列实验操作中数据合理的是( )
| A、用10mL量筒量取5.2mL盐酸 |
| B、用pH试纸测得某溶液的pH值为12.5 |
| C、用托盘天平称取25.12gNaCl固体 |
| D、用100mL容量瓶配制50mL0.1mol/L的盐酸 |
氮族元素与同周期的碳族、氧族元素相比较,下列变化规律正确的是( )
| A、原子半径:C<N<O |
| B、非金属性:Si>P>S |
| C、稳定性:SiH4>PH3>H2S |
| D、酸性强弱:H2SiO3<H3PO4<H2SO4 |