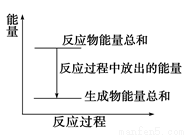
题目内容
已知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-  I3-)下列说法不正确的是
I3-)下列说法不正确的是
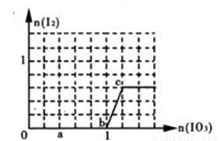
A.a点时消耗NaHSO3的物质的量为1.2mol,得到的氧化产物为SO42-
B.b~c段的反应可用如下离子方程式表示:IO3-+5I-+6H+=3I2+3H2O
C.滴加过程中水的电离平衡一直逆向移动。
D.从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏
练习册系列答案
相关题目
1.下列关于电化学的说法不正确的是( )
| A. | 两个隔离的不同半电池通过盐桥连接可以组成原电池 | |
| B. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | |
| C. | 在铁上镀银,用银作阳极 | |
| D. | 牺牲阳极的阴极保护法利用的是原电池原理 |


 Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示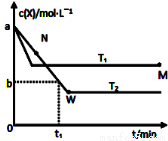
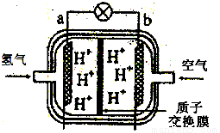

 ==ZnSO4(aq)+H2(g) ΔH<0的化学反应,下列叙述不正确的是
==ZnSO4(aq)+H2(g) ΔH<0的化学反应,下列叙述不正确的是