题目内容
下列反应的离子方程式中正确的是( )
| A、铁与盐酸的反应:2Fe+6H+=2Fe3++3H2↑ |
| B、铁与硫酸铜溶液反应:Fe+Cu2+=Fe2++Cu |
| C、向氢氧化铜中滴加硫酸溶液H++OH-=H2O |
| D、石灰石与稀HCl反应制备CO2:CO32-+2H+=H2O+CO2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、铁和盐酸反应生成氯化亚铁和氢气;
B、铁和硫酸铜反应生成铜和硫酸亚铁;
C、氢氧化铜和硫酸反应生成硫酸铜和水,氢氧化铜是难溶于水的物质;
D、石灰石主要成分为碳酸钙,难溶于水.
B、铁和硫酸铜反应生成铜和硫酸亚铁;
C、氢氧化铜和硫酸反应生成硫酸铜和水,氢氧化铜是难溶于水的物质;
D、石灰石主要成分为碳酸钙,难溶于水.
解答:
解:A、铁和盐酸反应生成氯化亚铁和氢气,反应的离子方程式:Fe+2H+=Fe2++H2↑,故A错误;
B、铁和硫酸铜反应生成铜和硫酸亚铁,反应的离子方程式Fe+Cu2+=Fe2++Cu,故B正确;
C、氢氧化铜和硫酸反应生成硫酸铜和水,氢氧化铜是难溶于水的物质,反应的离子方程式2H++Cu(OH)2=2H2O+Cu2+,故C错误;
D、石灰石主要成分为碳酸钙难溶于水,反应的离子方程式CaCO3+2H+=H2O+CO2↑+Ca2+,故D错误;
故选B.
B、铁和硫酸铜反应生成铜和硫酸亚铁,反应的离子方程式Fe+Cu2+=Fe2++Cu,故B正确;
C、氢氧化铜和硫酸反应生成硫酸铜和水,氢氧化铜是难溶于水的物质,反应的离子方程式2H++Cu(OH)2=2H2O+Cu2+,故C错误;
D、石灰石主要成分为碳酸钙难溶于水,反应的离子方程式CaCO3+2H+=H2O+CO2↑+Ca2+,故D错误;
故选B.
点评:本题考查了离子方程式书写方法和注意问题,主要是物质溶解性分析判断,反应实质理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
由-CH3、-OH、 、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )
、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )
 、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )
、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )| A、1种 | B、2种 | C、3种 | D、4种 |
下列判断错误的是( )
| A、酸性:HClO4>H2SO4>H3PO4 |
| B、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| C、沸点:I2>Br2>Cl2>F2 |
| D、沸点:HI>HBr>HCl>HF |
用括号内的试剂和方法除去下列各物质的少量杂质,不正确的是( )
| A、乙烷中含有乙烯(酸性高锰酸钾溶液,洗气) |
| B、乙醇中含有水(生石灰、蒸馏) |
| C、溴苯中含有溴(氢氧化钠溶液、分液) |
| D、苯中含有苯酚(浓溴水、过滤) |
下列离子方程式书写不正确的是( )
| A、少量CO2通入澄清石灰水中:CO2+Ca(OH)2=CaCO3↓+H2O |
| B、碳酸镁与稀硫酸反应:MgCO3+2H+=Mg2++H2O+CO2↑ |
| C、金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
| D、向小苏打溶液中加入盐酸溶液:HCO3-+H+=CO2↑+H2O |
已知[Co(NH3)6]3+为空间立体结构,Co3+位于立体中心,且每个NH3分子与Co3+距离相等.若其中二个NH3分子被Cl-取代,所形成的[Co(NH3)4Cl2]+的同分异构体数目为( )
| A、2种 | B、3种 | C、4种 | D、5种 |
具有下列电子排布式的原子中,原子半径最大的是( )
| A、1s22s22p63s23p2 |
| B、1s22s22p63s2 |
| C、1s22s22p2 |
| D、1s22s22p63s23p4 |
下列5种有机物:①2-甲基丙烷;②乙醇;③丙烷;④丁烷;⑤葡萄糖.按它们的沸点由高到低的顺序排列正确的是( )
| A、①②③④⑤ |
| B、⑤②④①③ |
| C、⑤④②①③ |
| D、③①②⑤④ |
下列说法中正确的是( )
| A、醇在Cu或Ag的催化作用下都可以氧化成醛 |
B、有机物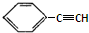 的所有原子一定处于同一平面上 的所有原子一定处于同一平面上 |
| C、醇都可以在浓H2SO4作用下以及170℃时发生消去反应 |
| D、分子组成相差一个或几个CH2原子团的化合物必定互为同系物 |