题目内容
下列说法中正确的是
- A.标准状况下,22.4L水中所含的分子数约为6.02×1023
- B.标准状况下,aL的氧气和氮气的混合物含有的分子数约为
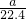 ×6.02×1023
×6.02×1023 - C.常温常压下,48gO3气体含有的氧原子数为6.02×1023
- D.2.24LCO2中含有的原子数为0.3×6.02×1023
B
分析:A、标况下水不是气态;
B、氮气和氧气均是双原子分子,根据N= NA来计算;
NA来计算;
C、根据氧原子数= NA×一个分子中氧原子数来计算;
NA×一个分子中氧原子数来计算;
D、Vm=22.4L/mol适用于标况下的气体.
解答:A、标况下水不是气态,Vm=22.4L/mol不适用,22.4L水的物质的量无法计算,所以22.4L水中所含的分子数不确定,故A错误;
B、标准状况下,aL的氧气和氮气的混合物含有的分子数N= NA=
NA=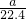 ×6.02×1023,故B正确;
×6.02×1023,故B正确;
C、常温常压下,48gO3中含有的氧原子数N= NA×一个分子中氧原子数=
NA×一个分子中氧原子数= NA=3NA=3×6.02×1023,故C错误;
NA=3NA=3×6.02×1023,故C错误;
D、Vm=22.4L/mol适用于标况下的气体,没指名状态,所以22.4L二氧化碳的物质的量不确定,原子数不确定,故D错误.
故选B.
点评:本题是一道关于阿伏加德罗常数的计算体,熟记宏观量和微观量之间的关系公式是解题的关键,难度不大.
分析:A、标况下水不是气态;
B、氮气和氧气均是双原子分子,根据N=
 NA来计算;
NA来计算;C、根据氧原子数=
 NA×一个分子中氧原子数来计算;
NA×一个分子中氧原子数来计算;D、Vm=22.4L/mol适用于标况下的气体.
解答:A、标况下水不是气态,Vm=22.4L/mol不适用,22.4L水的物质的量无法计算,所以22.4L水中所含的分子数不确定,故A错误;
B、标准状况下,aL的氧气和氮气的混合物含有的分子数N=
 NA=
NA=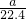 ×6.02×1023,故B正确;
×6.02×1023,故B正确;C、常温常压下,48gO3中含有的氧原子数N=
 NA×一个分子中氧原子数=
NA×一个分子中氧原子数= NA=3NA=3×6.02×1023,故C错误;
NA=3NA=3×6.02×1023,故C错误;D、Vm=22.4L/mol适用于标况下的气体,没指名状态,所以22.4L二氧化碳的物质的量不确定,原子数不确定,故D错误.
故选B.
点评:本题是一道关于阿伏加德罗常数的计算体,熟记宏观量和微观量之间的关系公式是解题的关键,难度不大.

练习册系列答案
相关题目