题目内容
14.实验室需要配制2.0mol•L-1的NaCl溶液500mL.(1)本实验所必需的仪器有托盘天平(精确到0.1g)、药匙、烧杯、量筒、玻璃棒、胶头滴管、500mL容量瓶 以及等质量的两片滤纸.
(2)某学生在摇匀后发现液面低于刻度线再加水,会导致结果偏低 (填“偏高”、“偏低”、“无影响”).
分析 (1)根据配制溶液的步骤操作选择所用仪器;
(2)分析操作对溶质物质的量、溶液体积的影响,根据c=$\frac{n}{V}$进行误差分析;
解答 解:(1)配制500mL2.0mol•L-1NaCl溶液,操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,用玻璃棒搅拌,加速溶解,恢复室温后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
所以需要的仪器有:托盘天平、烧杯、玻璃棒、500ml的容量瓶、胶头滴管、药匙,故还需要仪器为500ml的容量瓶,
故答案为:500ml的容量瓶;
(2)某学生在摇匀后发现液面低于刻度线再加水,导致溶液体积偏大,依据c=$\frac{n}{V}$可知,n不变,V增大,则溶液浓度偏低;
故答案为:偏低.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶规格选择及误差分析方法,题目难度不大.

练习册系列答案
相关题目
5.对H2O的电离平衡不产生影响的粒子是( )
| A. | HCl | B. | Fe3+ | C. | 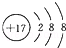 | D. | CH3COO- |
2.灭鼠灵是一种抗凝血型杀鼠剂,其结构如图.下列叙述不正确的是( )
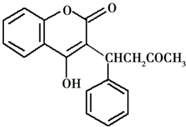

| A. | 灭鼠灵的分子式为C19H17O4 | |
| B. | 灭鼠灵可与溴水发身加成反应 | |
| C. | 分子中所有的碳原子都可能在同一个平面上 | |
| D. | 1 mol灭鼠灵最多可与8 mol H2 反应 |
9.下列反应中可加入还原剂进行的是( )
| A. | Zn→Zn2+ | B. | H2→H2O | C. | Cl2→Cl- | D. | CuO→CuCl2 |
19.有下列物质:①甲烷;②苯;③聚乙烯;④乙烯;⑤乙炔;⑥甲苯既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ④⑤ | B. | ②④⑤ | C. | ④⑤⑥ | D. | ③④⑤ |
6.下列说法不正确的是( )
| A. | 量取10.08 mL 0.1 mol•L-1 NaHCO3溶液用碱式滴定管量取 | |
| B. | 为测定新制氯水的 pH,用玻璃棒蘸取液体滴在 pH 试纸上,与标准比色卡对照即可 | |
| C. | 探究催化剂对 H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL 5%H2O2和1mL H2O,向另一支试管中加入2mL 5%H2O2和1mL FeCl3溶液,观察并比较实验现象 | |
| D. | 已知 4H++4I-+O2=2I2+2H2O,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol•L-1 KI 溶液、0.1 mol•L-1 稀硫酸外,还需要用到淀粉溶液 |
3.如表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -2 |
| A. | X、Y分别与W形成的化合物都具有两性 | |
| B. | Z、W在同一主族 | |
| C. | 气态氢化物的稳定性为H2W<H2Z | |
| D. | X和Y对应的氢氧化物的碱性强弱比较:X(OH)2<Y(OH)3 |
4.适当可以加热,只用一种试剂就可以鉴别的物质组是( )
| A. | NaCl、KNO3、AlCl3、Fe(NO3)3 | B. | Fe、FeO、CuO、FeS、CuS、MnO2 | ||
| C. | MgCl2、FeCl2、KCl、AlCl3、NH4Cl | D. | K2CO3、NaI、Na2CO3、NaCl、Na2SO4 |
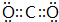 ,BA2分子中化学键属于共价键.
,BA2分子中化学键属于共价键. .
.