题目内容
10mL 0.1mol/LNH3?H2O中
(1)加水.则以下各值减小的有
A.c(OH-) B. c(NH3?H2O) C.n(NH4+)
D.n(NH3?H2O) E.n(OH-) F.c(OH-)/c(NH3?H2O)
(2)加热.同学甲认为n(NH4+)增大,同学乙认为n(NH4+)减小,你估计
甲的理由是:
乙的理由是:
(3)如果把氨水液面上方的空气换成氨气,则氨水中的氢氧根离子浓度如何变化,为什么?
, .
(1)加水.则以下各值减小的有
A.c(OH-) B. c(NH3?H2O) C.n(NH4+)
D.n(NH3?H2O) E.n(OH-) F.c(OH-)/c(NH3?H2O)
(2)加热.同学甲认为n(NH4+)增大,同学乙认为n(NH4+)减小,你估计
甲的理由是:
乙的理由是:
(3)如果把氨水液面上方的空气换成氨气,则氨水中的氢氧根离子浓度如何变化,为什么?
考点:弱电解质在水溶液中的电离平衡
专题:
分析:(1)加水稀释促进一水合氨电离,但一水合氨电离程度小于溶液体积增大程度,所以c(OH-)、c(NH3?H2O)、c(NH4+)都减小;
(2)一水合氨的电离是吸热反应,升高温度促进一水合氨电离;氨水易挥发,加热促进氨气逸出;
(3)气体溶解度随着压强的增大而增大.
(2)一水合氨的电离是吸热反应,升高温度促进一水合氨电离;氨水易挥发,加热促进氨气逸出;
(3)气体溶解度随着压强的增大而增大.
解答:
解:(1)加水稀释促进一水合氨电离,则n(NH3?H2O)减小、n(OH-)和n(NH4+)增大,
但一水合氨电离程度小于溶液体积增大程度,所以c(OH-)、c(NH3?H2O)、c(NH4+)都减小,
则c(OH-)/c(NH3?H2O)增大,故选ABD;
(2)甲:一水合氨的电离是吸热反应,升高温度促进一水合氨电离,则n(NH4+)增大;
乙:氨水易挥发,加热促进氨气逸出,抑制一水合氨电离,所以n(NH4+)减小,
故答案为:氨水的电离是一个吸热过程,温度升高,促进氨水电离,n(NH4+)增大;氨水易挥发,温度升高氨气逸出,电离平衡左移,n(NH4+)减小
(3)氨气气压增大,NH3(g)+H2O?NH3?H2O(aq),NH3?H2O(aq)?NH4+(aq)+OH-(aq)平衡右移,碱性增强,pH增大,故答案为:增大;氨气气压增大,NH3(g)+H2O?NH3?H2O(aq),NH3?H2O(aq)?NH4+(aq)+OH-(aq)平衡右移,碱性增强,pH增大.
但一水合氨电离程度小于溶液体积增大程度,所以c(OH-)、c(NH3?H2O)、c(NH4+)都减小,
则c(OH-)/c(NH3?H2O)增大,故选ABD;
(2)甲:一水合氨的电离是吸热反应,升高温度促进一水合氨电离,则n(NH4+)增大;
乙:氨水易挥发,加热促进氨气逸出,抑制一水合氨电离,所以n(NH4+)减小,
故答案为:氨水的电离是一个吸热过程,温度升高,促进氨水电离,n(NH4+)增大;氨水易挥发,温度升高氨气逸出,电离平衡左移,n(NH4+)减小
(3)氨气气压增大,NH3(g)+H2O?NH3?H2O(aq),NH3?H2O(aq)?NH4+(aq)+OH-(aq)平衡右移,碱性增强,pH增大,故答案为:增大;氨气气压增大,NH3(g)+H2O?NH3?H2O(aq),NH3?H2O(aq)?NH4+(aq)+OH-(aq)平衡右移,碱性增强,pH增大.
点评:本题考查了弱电解质的电离,明确弱电解质的电离特点及影响弱电解质电离因素即可解答,注意:加水稀释促进一水合氨电离但溶液中c(OH-)、c(NH3?H2O)、C(NH4+)都减小,氢离子浓度增大,为易错点.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
下列碱金属(IA族中的金属)性质的递变规律,随着核电荷数的递增,下列叙述错误的是( )
| A、单质的熔沸点依次升高 |
| B、原子半径依次增大 |
| C、单质的还原性依次增强 |
| D、氧化物对应的水化物碱性依次增强 |
结构为 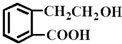 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:
①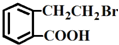 ②
②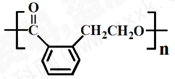 ③
③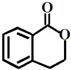 ④
④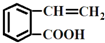
生成这四种有机物的反应类型依次为( )
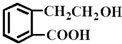 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:①
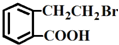 ②
② ③
③ ④
④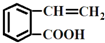
生成这四种有机物的反应类型依次为( )
| A、酯化、取代、缩聚、取代 |
| B、取代、取代、加聚、消去 |
| C、取代、缩聚、酯化、消去 |
| D、取代、加成、酯化、消去 |
下列叙述正确的是( )
| A、只有在标准状况下,48 g O3气体才含有6.02×1023个O3分子 |
| B、常温常压下,4.6 gNO2气体约含有1.81×1023个原子 |
| C、0.5 mol?L-1CuCl2溶液中含有Cu2+数小于3.01×1023个 |
| D、标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
下列说法正确的是( )
| A、物质失去电子数越多,物质的还原性越强 |
| B、导电的不一定是电解质,电解质不一定导电 |
| C、得到电子的物质是还原剂 |
| D、还原剂反应后得到是还原产物 |
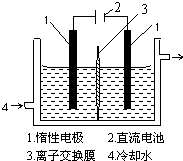 在全民补碘政策实施了15年之久的今天,有媒体报道称,一些地区的临床医生反映甲状腺疾病发病呈上升趋势,于是一些专家呼吁,停止对食盐进行国家的强制加碘,应该根据不同地区的实际情况来决定是否应该加碘.食盐加碘剂主要成份是碘酸钾(KIO3).工业上可用碘为原料通过电解制备碘酸钾.
在全民补碘政策实施了15年之久的今天,有媒体报道称,一些地区的临床医生反映甲状腺疾病发病呈上升趋势,于是一些专家呼吁,停止对食盐进行国家的强制加碘,应该根据不同地区的实际情况来决定是否应该加碘.食盐加碘剂主要成份是碘酸钾(KIO3).工业上可用碘为原料通过电解制备碘酸钾.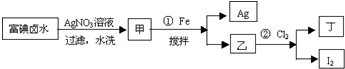
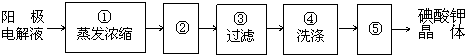
 i.
i. j.
j. k.
k.