题目内容
(Ⅰ)(7分)
甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,
则甲醇燃烧的热化学方程式为 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2
已知H2(g)+ O2(g)===H2O(g) △H =-241.8 kJ·mol-1
O2(g)===H2O(g) △H =-241.8 kJ·mol-1
则反应②的△H2= kJ·mol-1。
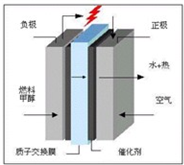
(3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),写出正极的电极反应式

(Ⅱ)(5分)
铅蓄电池是典型的可充型电池,它的正负极隔板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO42-  2PbSO4+2H2O,请回答下列问题(不考虑氢、氧的氧化还原):
2PbSO4+2H2O,请回答下列问题(不考虑氢、氧的氧化还原): 
(1)放电时:正极的电极反应式是
电解液中H2SO4的浓度将变 ;
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成 B电极上生成
(Ⅰ)
(1)CH3OH(l) + 3/2 O2(g) === CO2(g) + 2H2O(l) △H =-726.51 kJ/mol (2分)
(2)-192.8 (2分)
(3)负 O2 + 4H+ + 4e-=== 2H2O (3分)
(Ⅱ)(1)PbO2+2e-+4H++SO42-=PbSO4+2H2O 小 (3分)
(2)Pb PbO2(2分)
【解析】略

 口算能手系列答案
口算能手系列答案①2CH4(g)+O2(g)=2CO(g)+4H2(g);△H=-71kJ?mol-1
②CO(g)+2H2(g)=CH3OH(l);△H=-90.5kJ?mol-1
下列描述错误的是( )
| A、CO(g)+2H2(g)═CH3OH(g)△H>-90.5kJ?mol-1 | ||
| B、在甲醇燃料电池中,甲醇所在电极为正极 | ||
C、CH4(g)+
| ||
D、 反应①中的能量变化如图所示 |

 CH3OH(g)△H1=-116kJ?molˉ1
CH3OH(g)△H1=-116kJ?molˉ1
 化的曲线图,请指明图中的压强P1=
化的曲线图,请指明图中的压强P1= CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为 2012年 12 月7日,日本发生7.3级地震,大地震引起的核泄漏阴影再次引起了人们对核能源的恐慌.各国都在寻找替代核能的新型能源,而甲醇是未来重要的绿色能源之一.
2012年 12 月7日,日本发生7.3级地震,大地震引起的核泄漏阴影再次引起了人们对核能源的恐慌.各国都在寻找替代核能的新型能源,而甲醇是未来重要的绿色能源之一.