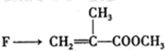题目内容
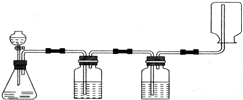 某学生在实验室做气体发生、洗涤、干燥、收集(不考虑尾气的处理)实验,装置图如图示.该同学所做的实验是( )
某学生在实验室做气体发生、洗涤、干燥、收集(不考虑尾气的处理)实验,装置图如图示.该同学所做的实验是( )| A、锌和盐酸反应制取氢气 |
| B、二氧化锰和浓盐酸反应制取氯气 |
| C、碳酸钙和盐酸反应制取二氧化碳 |
| D、过氧化钠和水反应制取氧气 |
考点:实验装置综合
专题:实验设计题
分析:根据装置图可知该气体制取是固体和液体不需加热的反应,能用向下排气法收集,说明生成的气体的密度比比空气的密度小且不会和空气中的成分反应,据此分析解答.
解答:
解:A.锌和盐酸发生反应无需加热,生成的氢气的密度比空气小,能用向下排气法收集,符合上述要求,故A正确;
B.二氧化锰和浓盐酸反应制取氯气需要加热,而且氯气的密度比空气大,收集方法应用向上排气法,故B错误;
C.碳酸钙和盐酸生成二氧化碳,制备装置符合,二氧化碳的密度比空气大,收集方法应用向上排气法,故C错误;
D.过氧化钠和水反应制取氧气,在常温下进行,制备装置符合,但是氧气的密度比空气大,收集方法应用向上排气法,故D错误;
故选A.
B.二氧化锰和浓盐酸反应制取氯气需要加热,而且氯气的密度比空气大,收集方法应用向上排气法,故B错误;
C.碳酸钙和盐酸生成二氧化碳,制备装置符合,二氧化碳的密度比空气大,收集方法应用向上排气法,故C错误;
D.过氧化钠和水反应制取氧气,在常温下进行,制备装置符合,但是氧气的密度比空气大,收集方法应用向上排气法,故D错误;
故选A.
点评:本题考查了常见气体实验室制备的原理、除杂、收集等知识的运用,重点考查装置的选择,除杂试剂的选择,收集气体的方法,题目难度不大.

练习册系列答案
相关题目
在标准状况下,下列物质的体积最大的是( )
| A、2gH2 |
| B、22gCO2 |
| C、23gNa |
| D、36gH2O |
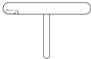 人们常用如右图所示仪器反复进行某物质的性质实验,如碘的升华实验.用该仪器能反复进行的还有:( )
人们常用如右图所示仪器反复进行某物质的性质实验,如碘的升华实验.用该仪器能反复进行的还有:( )①NH4Cl受热分解实验
②KClO3受热分解实验
③CuSO4和CuSO4?5H2O的互变实验
④Fe(OH)3受热分解实验.
| A、②④ | B、①③ | C、①④ | D、②③ |
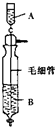 《Inorganic Syntheses》(无机合成)一书中,有一如图所示的装置,用以制备某种干燥的纯净气体.该装置中所装的药品正确的是( )
《Inorganic Syntheses》(无机合成)一书中,有一如图所示的装置,用以制备某种干燥的纯净气体.该装置中所装的药品正确的是( )| A、A中装浓盐酸,B中装浓硫酸 |
| B、A中装浓硫酸,B中装浓盐酸 |
| C、A中装氢氧化钠浓溶液,B中装浓氨水 |
| D、A中装浓氨水,B中装氢氧化钠浓溶液 |
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验中配制1mol?L-1的稀硫酸标准,然后用其滴定某未知浓度的氢氧化钠溶液.下列有关说法中正确的是( )
| A、实验中所用到的锥形瓶和容量瓶,在洗涤后均需要润洗 |
| B、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,最终氢氧化钠溶液浓度将偏大 |
| C、滴定时,左手提酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视滴定管内液面变化 |
| D、中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大 |
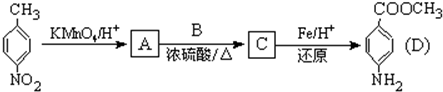
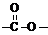 结构的基团的C的所有同分异构体的结构简式:
结构的基团的C的所有同分异构体的结构简式: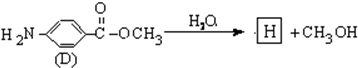
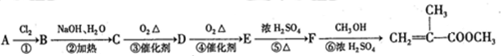 ,
,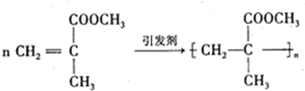
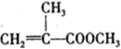 是有机玻璃的单体.下列物质属甲基丙烯酸甲酯同分异构体的是
是有机玻璃的单体.下列物质属甲基丙烯酸甲酯同分异构体的是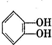 、④
、④