题目内容
下列说法中正确的是( )
| A、CO2、NH3、CCl4、N2中,所有原子都满足最外层8电子的稳定结构 | B、在元素周期表中金属和非金属交界处可以找到半导体材料 | C、共价化合物可能含离子键 | D、第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键 |
分析:A.氢原子最多满足最为最外层两电子结构;
B.在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料;
C.含离子键的化合物一定是离子化合物,共价化合物中一定不存在离子键;
D.氢和第ⅦA族元素的原子之间形成共价键.
B.在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料;
C.含离子键的化合物一定是离子化合物,共价化合物中一定不存在离子键;
D.氢和第ⅦA族元素的原子之间形成共价键.
解答:解:A.氢原子最多满足最为最外层两电子结构,故氨气中氢原子没达到8电子稳定结构,故A错误;
B.在金属元素和非金属元素交接区域的元素通常既具有金属性又具有非金属性,可以用来做良好的半导体材料,如硅等,故B正确;
C.含离子键的化合物一定是离子化合物,共价化合物中一定不存在离子键,故C错误;
D.第ⅠA族氢元素和第ⅦA族元素的原子之间形成共价键,故D错误;
故选B.
B.在金属元素和非金属元素交接区域的元素通常既具有金属性又具有非金属性,可以用来做良好的半导体材料,如硅等,故B正确;
C.含离子键的化合物一定是离子化合物,共价化合物中一定不存在离子键,故C错误;
D.第ⅠA族氢元素和第ⅦA族元素的原子之间形成共价键,故D错误;
故选B.
点评:本题考查了原子结构、元素周期表应用及化学键类型判断,中等难度.注意氢元素原子结构的特殊性及氢元素在周期表的位置.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法中正确的是( )
| A、进行钠的有关性质实验时,用剩的钠应放回原试剂瓶 | B、常用25.00 ml 碱式滴定管准确量取20.00 ml KMnO4溶液 | C、用湿润的淀粉碘化钾试纸可以鉴别NO2和Br2蒸气 | D、某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
Na3N和NaH都是离子化合物,与水反应都有气体生成,下列说法中正确的是( )
| A、两种物质的阴离子半径都比阳离子半径小 | B、溶于水,所得溶液都能使无色酚酞变红 | C、与水反应时,水都做氧化剂 | D、与盐酸反应都只生成一种盐 |
下列说法中正确的是( )
| A、用碱石灰除去氯气中的水 | B、碘化银是重要的感光材料,溴化银可用于人工降雨 | C、过氧化钠可用作潜艇里氧气的来源 | D、焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察 |
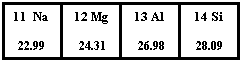 如图为元素周期表第三周期的一部分.据此判断下列说法中正确的是( )
如图为元素周期表第三周期的一部分.据此判断下列说法中正确的是( )| A、Si元素的名称是硅,其核电荷数为14 | B、Mg原子的结构示意图是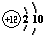 | C、Al的相对原子质量是26.98g | D、它们都属于金属元素 |
下列说法中正确的是( )
| A、O、Na、S元素的原子半径依次增大 | B、KOH、Mg(OH)2、Ba(OH)2的碱性依次增强 | C、H2SO4、H3PO4、HClO4的酸性依次增强 | D、F2、Cl2、Br2、I2的氧化性依次减弱 |