题目内容
某同学发现在灼热的煤炭上洒少量水,煤炉中会产生淡蓝色火焰,煤炭燃烧更旺,(已知煤炭的燃烧热为393kJ/mol,氢气的燃烧热为242kJ/mol,一氧化碳的燃烧热为283kJ/mol)
(1)写出各燃烧热的热化学反应方程式; .
(2)写出“灼热的煤炭上洒少量水”的反应的热化学方程式: .
(1)写出各燃烧热的热化学反应方程式;
(2)写出“灼热的煤炭上洒少量水”的反应的热化学方程式:
考点:热化学方程式
专题:
分析:(1)依据燃烧热的概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量;结合反应的热化学方程式书写方法写出,注意标注物质的聚集状态,对应化学方程式量下的反应热;
(2)单质碳在高温下可以和水反应得到一氧化碳和氢气,根据盖斯定律计算反应热,写出碳和水蒸气反应的热化学方程式.
(2)单质碳在高温下可以和水反应得到一氧化碳和氢气,根据盖斯定律计算反应热,写出碳和水蒸气反应的热化学方程式.
解答:
解:(1)已知煤炭的燃烧热为-393.15kJ/mol,氢气的燃烧热为-242kJ/mol,一氧化碳的燃烧热为-283kJ/mol;上述反应过程中包括碳燃烧、碳和水的反应,氢气燃烧,一氧化碳燃烧,依据燃烧热概念写出热化学方程式:
①C (s)+O2(g)=CO2(g)△H=-393.15 kJ/mol;
②H2(g)+
O2 (g)=H2O (l)△H=-285.8kJ/mol
③CO (g)+
O2 (g)=CO2(g)△H=-283 kJ/mol
故答案为:①C (s)+O2(g)=CO2(g)△H=-393.15 kJ/mol
②H2(g)+
O2 (g)=H2O (l)△H=-285.8kJ/mol
③CO (g)+
O2 (g)=CO2(g)△H=-283 kJ/mol;
(2)单质碳在高温下可以和水反应得到一氧化碳和氢气,依据盖斯定律,①-②-③得到:C(s)+H2O (l)=CO(g)+H2 (g)△H=+175.65 kJ/mol,
故答案为:C(s)+H2O (l)=CO(g)+H2 (g)△H=+175.65 kJ/mol.
①C (s)+O2(g)=CO2(g)△H=-393.15 kJ/mol;
②H2(g)+
| 1 |
| 2 |
③CO (g)+
| 1 |
| 2 |
故答案为:①C (s)+O2(g)=CO2(g)△H=-393.15 kJ/mol
②H2(g)+
| 1 |
| 2 |
③CO (g)+
| 1 |
| 2 |
(2)单质碳在高温下可以和水反应得到一氧化碳和氢气,依据盖斯定律,①-②-③得到:C(s)+H2O (l)=CO(g)+H2 (g)△H=+175.65 kJ/mol,
故答案为:C(s)+H2O (l)=CO(g)+H2 (g)△H=+175.65 kJ/mol.
点评:本题考查了物质燃烧热的概念应用,盖斯定律的分析应用,题目较简单.

练习册系列答案
相关题目
下列有关化学实验安全问题的叙述中不正确的是( )
| A、实验室制备有毒气体应在通风橱中进行,且必须对尾气进行吸收或处理 |
| B、浓硝酸需用细口棕色试剂瓶密封保存 |
| C、氢气还原氧化铜,一般先预热氧化铜,然后通入氢气 |
| D、高锰酸钾等药品不能和易燃物同放,且远离火源 |
关于电解质和非电解质的说法中正确的是( )
| A、电解质一定能导电 |
| B、某物质不是电解质就是非电解质 |
| C、非电解质在水溶液中也可能会发生电离 |
| D、强电解质在水溶液中完全以离子形式存在 |
将NaHSO4溶液和NaHCO3溶液混合,发生反应的离子方程式为( )
| A、H++HCO3-═H2O+CO2↑ |
| B、2HSO4-+CO32-═H2O+CO2↑+2SO42- |
| C、HSO4-+HCO3-═H2O+CO2↑+SO42- |
| D、2H++CO32-═H2O+CO2↑ |
对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4下列关于该反应的说法正确的是( )
| A、CuSO4发生了氧化反应 |
| B、生成1 mol H3PO4时,有10 mol 电子转移 |
| C、白磷只作还原剂 |
| D、氧化产物和还原产物的物质的量之比为6:5 |
20g密度为dg/cm3的硝酸钙溶液中,含有1gCa2+离子,则NO3-离子的物质的量浓度为( )
A、
| ||
B、
| ||
| C、2.5dmol/L | ||
| D、1.25dmol/L |
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
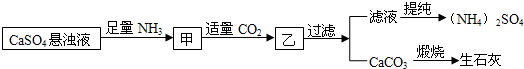
下列推断不合理的是( )

下列推断不合理的是( )
| A、生成1mol (NH4)2SO4至少消耗2mol NH3 |
| B、CO2可被循环使用 |
| C、先通二氧化碳,后通氨气,效果相同 |
| D、往甲中通CO2有利于制备(NH4)2SO4 |