��Ŀ����
14������װ�г��������������Ϊ��ԭ�����ۡ��Ȼ��ơ�̿�۵ȣ�������ԭ���������������ʴ��ͬ�����з�����ȷ���ǣ�������| A�� | �������������ȷ�ӳ���ɽ����¶ȣ��ӳ���㱣���� | |
| B�� | ��������������ԭ��ظ������缫��ӦΪ��Fe-3e-��Fe3+ | |
| C�� | ��������������ת��Ϊ��������ڲ����� | |
| D�� | ��״������������336mL������������Ҫ����1.12g���۵������� |
���� Fe��C��NaCl��Һ����ԭ��أ�����������ʴ��Fe��ʧ������������C��������������ӦʽΪFe-2e-=Fe2+��������ӦʽΪ2H2O+O2+4e-=4OH-�����ɵ��������Ӻ����������ӷ�Ӧ�������������������������������������������������ݵ缫��Ӧ�Լ������غ���м��㼴�ɣ�
��� �⣺A����װ�ù���ԭ��أ�ԭ��ط�ӦΪ���ȷ�Ӧ������ȥ��������Ϊ���ȷ�Ӧ����A����
B����������������ԭ��ظ������缫��ӦΪ��Fe-2e-=Fe2+����B����
C���������������ʷ�Ӧ�Ļ�ѧ��ת��Ϊ���ܺ����ܣ���C����
D��������ӦʽΪFe-2e-=Fe2+��������ӦʽΪ2H2O+O2+4e-=4OH-�����ɵ��������Ӻ����������ӷ�Ӧ��������������������������������������������������Fe��������ת��Ϊ+3����Ԫ�أ���״������������336mL��0.015mol��ת�Ƶ��ӵ����ʵ���Ϊ0.06mol������ת�Ƶ����غ���������������0.02mol��56g/mol=1.12g����D��ȷ��
��ѡD��
���� ���⿼�������ʴ���������ȷ����ʴ�����з����ķ�Ӧ�ǽⱾ��ؼ����״�ѡ����B��ע�����������ձ������������ʵijɷ��ǽⱾ��ؼ���Ϊ�״��㣮

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���1������ͭ��Һ���Լӿ������������ʵ�ԭ����CuSO4��Zn��Ӧ������Cu��Zn�γ�Cu/Znԭ��أ��ӿ����������������ʣ�
��2��ʵ����������Na2SO4��MgSO4��Ag2SO4��K2SO4��4����Һ������ʵ����CuSO4��Һ���������õ���Ag2SO4��
��3��Ҫ�ӿ�����ʵ����������������ʣ����ɲ�ȡ�Ĵ�ʩ�����߷�Ӧ�¶ȡ��ʵ����������Ũ�ȡ�����п���ıȱ�����ȣ������֣���
��4��Ϊ�˽�һ���о�����ͭ�����������������ʵ�Ӱ�죬��ͬѧ���������һϵ��ʵ�飮�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���ķ�Ӧƿ�У��ռ����������壬��¼�����ͬ�������������ʱ�䣮
| ʵ�� �����Һ | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| ����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
�ڸ�ͬѧ���ó��Ľ���Ϊ������������CuSO4��Һʱ���������������ʻ�����ߣ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���������������������½�����Ҫԭ����һ������CuSO4�����ɵĵ���Cu�������Zn�ı��棬������Zn����Һ�ĽӴ������
| A�� | C+O2�TCO2 | B�� | NH3+HCl�TNH4Cl | ||
| C�� | 2Fe��OH��3�TFe2O3+3H2O | D�� | NaOH+HNO3�TNaNO3+H2O |
������0.50mol•L-1NaOH��Һ
��1������0.50mol•L-1NaOH��Һʱ����Ҫʹ�õIJ�����������Ͳ���ձ����������⣬����250ml����ƿ����ͷ�ιܣ�
��2����ʵ����Լ��Ҫ240ml0.50mol•L-1NaOH��Һ����Ӧ����Ͳ��ȡ2.5mol•L-1NaOH��Һ�����Ϊ50.0ml��
�ⶨ�к���
ȡ60mL NaOH��Һ��40mL������Һ����ʵ�飬ʵ�����������
| ʵ�� ���� | ��ʼ�¶�t1/�� | ��ֹ�¶� t2/�� | ||
| H2SO4 | NaOH | ƽ��ֵ ������С�����һλ�� | ||
| 1 | 26.3 | 26.0 | 26.1 | 30.1 |
| 2 | 27.0 | 27.3 | 27.2 | 33.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.5 | 26.2 | 26.3 | 30.4 |
��4������ʵ����ֵ�����57.3kJ•mol-1��ƫ�������ƫ���ԭ�����ad������ĸ����
a��ʵ��װ�ñ��¡�����Ч����
b����ȡ40mL0.50mol•L-1����ʱ���Ӷ���
c�����ᵹ��С�ձ�ʱ�����������ὦ��
d�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
��5���ֽ�һ������ϡ����������Һ��ϡ����������Һ��ϡ��ˮ�ֱ��1L 0.50mol/L��ϡ����ǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�Ϊ��H1����H2����H3�����H1����H2����H3�ɴ�С�Ĺ�ϵΪ��H3����H1����H2��
| ѡ�� | ������ | ������ |
| A | SO2��ʹ��ˮ��ɫ | SO2���л�ԭ�� |
| B | NH3��ʹ��̪��Һ��� | NH3�����������Ȫ |
| C | SiO2��������ᡢ�Ӧ | SiO2������������ |
| D | ����Si�۵��Ӳ�ȴ� | ����Si�������뵼����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | M g | B�� | $\frac{1}{M}$g | C�� | $\frac{6.02��1{0}^{23}}{M}$g | D�� | $\frac{M}{{N}_{A}}$g |
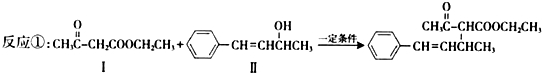
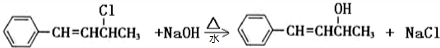 ��
��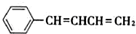 ��
��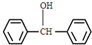 ��
��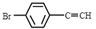 ��Ҳ���Է������Ʒ�Ӧ�ٵķ�Ӧ���л�����Ľṹ��ʽΪ
��Ҳ���Է������Ʒ�Ӧ�ٵķ�Ӧ���л�����Ľṹ��ʽΪ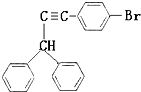 ��
��