题目内容
下列各组无色溶液中,能大量共存的离子组是( )
| A、K+、H+、SO42-、OH- |
| B、Na+、K+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、K+、Cu2+、SO42-、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应,则离子大量共存,并结合离子的颜色来解答.
解答:
解:A.H+、OH-结合生成水,不能大量共存,故A不选;
B.该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.H+、CO32-结合生成水和气体,不能大量共存,故C不选;
D.Cu2+为蓝色,与无色不符,故D不选;
故选B.
B.该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.H+、CO32-结合生成水和气体,不能大量共存,故C不选;
D.Cu2+为蓝色,与无色不符,故D不选;
故选B.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应及常见离子颜色的考查,题目难度不大.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
标准状况下22.4LH2 和C2H4的混合气体在一定条件下反应,所得气态物质完全燃烧恢复至常温后放出736KJ热量,混合气体中H2和C2H4的物质的量之比应为[已知H2、C2H4、C2H6的燃烧热(单位:KJ/mol)分别是286、1411和1560]( )
| A、1:3 | B、2:3 |
| C、3:1 | D、3:2 |
从柑桔中炼制出有机物 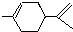 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )
 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )| A、分子式为C10H16 |
| B、常温下为液态,难溶于水 |
| C、属于芳香烃 |
| D、1mol该物质与1molHCl加成所得产物有四种 |
在某容器中,C+H2O(g)?CO+H2反应达到平衡,在温度、体积不变的情况下,向容器中充入一定量H2,当建立新平衡时( )
| A、CO、H2的浓度都比原平衡时的要小 |
| B、CO、H2的浓度都比原平衡时的要大 |
| C、H2、H2O(g)的浓度都比原平衡时的要大 |
| D、CO、H2O(g)的浓度都比原平衡时的要大 |
下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是( )
| A、H2SO4 |
| B、KOH |
| C、BaCl2 |
| D、Na2CO3 |
下列说法正确的是( )
| A、一定温度下,当弱酸的浓度相同时,电离常数越大,酸性越强 |
| B、合成氨的反应,正反应的平衡常数和逆反应的平衡常数相同 |
| C、实验测定酸碱滴定曲线时,要保证整个过程测试和记录pH的间隔相同 |
| D、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
常温下,向等物质的量浓度的两种一元酸的盐溶液中,分别通入少量的CO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3;2NaB+CO2+H2O=2HB+Na2CO3,则等物质的量浓度的HA和HB在水中电离出H+的能力大小关系是( )
| A、HA较强 | B、HB较强 |
| C、两者一样 | D、无法比较 |
下列说法不正确的是( )
| A、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
| B、用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| D、分子式为C4H10O并能与金属钠反应放出氢气的有机化合物有4种 |
下列说法正确的是( )
| A、实验室配制240mL2.0mol/L的NaOH溶液,应称NaOH晶体19.2g |
| B、为防止药品污染,用剩的金属钠放入垃圾桶中 |
| C、用25 mL量筒量取22.6 mL盐酸 |
| D、用托盘天平称取8.75 g食盐 |